题目内容
【题目】氨水和盐酸是常见的化学试剂,可将氨气(NH3)、氯化氢气体分别溶于水制得。(1)工业上利用氮气和氢气反应制氨气,反应的化学方程式为 (不要求注明条件)。
(2)小华为探究氨气溶于水是否发生化学反应,设计并完成如下实验(填写表中空白):
实验操作 | 实验现象及结论 |
将浸有酚酞溶液的滤纸干燥后,放入盛有干燥氨气的集气瓶中 | 无明显现象 |
(3)小明将滴有酚酞的稀氨水加热,观察到溶液颜色变浅,原因可能是 。
(4)小芳将滴有石蕊的稀盐酸加热,溶液颜色无明显变化。为进一步研究,取稀盐酸分成2份:①未经加热;②加热煮沸一段时间后冷却,分别中和等量的氢氧化钠,消耗二者的质量:①﹥②,则稀盐酸经加热煮沸后浓度 (填“增大”、“减小”或“不变”)。
【注意:若答对(5)小题奖励4分,化学试卷总分不超过60分。】
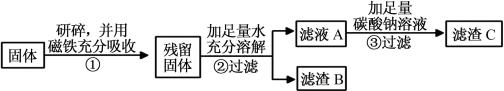
(5)为除去氯化钠溶液中的碳酸钠,小林设计了如下方案:
![]()
你认为上述方案 (填“合理”或“不合理”),请分析: (如合理,说明原因;如不合理,说明原因并设计改进方案)。
【答案】(1)N2+3H2==2NH3 (2)①向上述集气瓶中滤纸上滴入少量水(合理答案即可)
②滤纸变红,说明二者发生了反应 (3)氨水受热分解速度加快,分解出氨气或随温度升高氨气溶解度减小,导致氨水浓度降低(合理答案即可) (4)增大 (5)不合理 根据上述实验,加热煮沸无法除去溶液A中混有的过量氯化氢。改进方案:向含碳酸钠的氯化钠溶液中边逐滴加盐酸,边测定溶液的pH,至溶液呈中性即可(合理答案即可)
【解析】
试题分析:(1)氮气和氢气反应的化学方程式为:N2+3H2==2NH3 (2)做对比实验要主要控制变量,故①向上述集气瓶中滤纸上滴入少量水 ②滤纸变红,说明二者发生了反应 (3)氨水受热分解速度加快,分解出氨气或随温度升高氨气溶解度减小,导致氨水浓度降低 (4)①未经加热;②加热煮沸一段时间后冷却,分别中和等量的氢氧化钠,消耗二者的质量:①﹥②,说明消耗加热煮沸的稀盐酸溶液少,则稀盐酸经加热煮沸后浓度增大

 本土教辅赢在暑假高效假期总复习云南科技出版社系列答案
本土教辅赢在暑假高效假期总复习云南科技出版社系列答案 暑假作业北京艺术与科学电子出版社系列答案
暑假作业北京艺术与科学电子出版社系列答案 第三学期赢在暑假系列答案
第三学期赢在暑假系列答案