题目内容
复习时,常用专题探究的方法学习常见物质的组成、性质与制取.探究1:研究常见物质组成
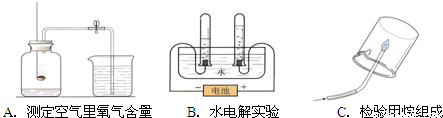
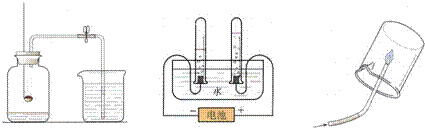
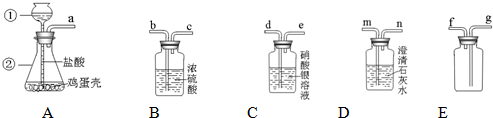
A、B、C都是研究物质组成的实验.从研究方法得知,A实验是利用可燃物消耗瓶内的______,使瓶内压强减小来推测空气里氧气的含量.B实验推断出水由氢、氧元素组成的依据是______.C的实验依据与______(填实验代号)实验依据相同.
探究2:研究常见物质性质--氢氧化钠与硫酸是否刚好完全中和
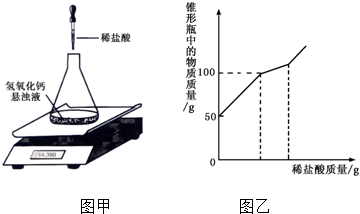
(1)探索:用玻璃棒蘸取反应后的溶液滴在pH试纸上,该溶液的pH<7,说明硫酸过量.
(2)验证:
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中,______ | ______ | 证明研究结论正确 |
探究3:研究常见物质制取--制取氢氧化钠溶液
小张同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”小李认为小张的实验不严密,其理由是______.他设计了另一个实验来证明该无色溶液中确实含有氢氧化钠.请你帮他完成下列实验报告:
| 实验步骤 | 实验现象 | 实验结论 |
| ______ | ______ | 无色溶液中确实 含有氢氧化钠 |
【答案】分析:探究1:这三个实验都是研究物质组成的实验,其中A实验是通过消耗氧气的体积来测定空气中氧气的含量,B、C是利用质量守恒定律来通过生成物的组成来推断反应物的组成.
探究2:主要的验证酸的存在,根据酸的化学性质,可以选择金属,碱,盐等物质,只要有明显的现象就可以,可以据此来解答该题;
探究3:根据只要溶液显碱性就会使酚酞变红进行判断分析小李的理由,若证明它们确实反应生成了氢氧化钠,应该排除碳酸钠的干扰,可以据此设计实验来进行验证.
解答:解:探究1:A实验中氧气有助燃性,白磷燃烧要消耗集气瓶中的氧气,从而使集气瓶中压强减小,烧杯中的水在外界大气压的作用下进入集气瓶,进入集气瓶中的水的体积等于集气瓶中原来氧气的体积;
B实验是电解水的试验,通过验证两个试管中的气体,再结合反应前后元素种类不变的原则,就可以确定组成水的元素;
C实验是验证甲烷元素组成的实验,通过验证甲烷燃烧的产物,再结合反应前后元素种类不变的原则,就可以确定甲烷的元素组成,故原理和B的一致;
探究2:用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现该溶液的pH<7,说明硫酸过量,要证明硫酸过量,根据酸的化学性质,可以用金属和酸反应,能放出气泡;可以和碱反应,不溶性碱能溶于酸;可以和盐反应,碳酸盐遇酸生成二氧化碳气体;
探究3:因为只要是碱性的溶液就能使无色酚酞变成红色,因为碳酸钠溶液显碱性,也会使无色酚酞变红色,所以不能仅仅根据溶液变红就判断制得了氢氧化钠,为了更具有说服力应该排除碳酸钠的干扰,即除去碳酸钠,根据碳酸钠的性质可以选用硝酸钡,氯化钡等溶液,然后过滤,在向滤液中加入酚酞根据溶液颜色的变红来判断.
故答案为:探究1:氧气;生成物含有氢元素和氧元素(反应前后元素种类不变);B;
探究2:
Zn+H2SO4═ZnSO4+H2↑(或CuO+H2SO4═CuSO4+H2O或Cu(OH)2+H2SO4═CuSO4+2H2O或Na2CO3+H2SO4═Na2SO4+H2O+CO2↑);
探究3:碳酸钠溶液也能使无色酚酞试液变红(或碳酸钠溶液也显碱性);
点评:探究物质的组成方法比较多,本题通过三种方法来验证物质的组成,同学们要根据实际情况进行应用,同时要熟练掌握酸碱盐的性质,知道碳酸钠虽然是盐,但是其溶液呈碱性.
探究2:主要的验证酸的存在,根据酸的化学性质,可以选择金属,碱,盐等物质,只要有明显的现象就可以,可以据此来解答该题;
探究3:根据只要溶液显碱性就会使酚酞变红进行判断分析小李的理由,若证明它们确实反应生成了氢氧化钠,应该排除碳酸钠的干扰,可以据此设计实验来进行验证.
解答:解:探究1:A实验中氧气有助燃性,白磷燃烧要消耗集气瓶中的氧气,从而使集气瓶中压强减小,烧杯中的水在外界大气压的作用下进入集气瓶,进入集气瓶中的水的体积等于集气瓶中原来氧气的体积;
B实验是电解水的试验,通过验证两个试管中的气体,再结合反应前后元素种类不变的原则,就可以确定组成水的元素;
C实验是验证甲烷元素组成的实验,通过验证甲烷燃烧的产物,再结合反应前后元素种类不变的原则,就可以确定甲烷的元素组成,故原理和B的一致;
探究2:用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现该溶液的pH<7,说明硫酸过量,要证明硫酸过量,根据酸的化学性质,可以用金属和酸反应,能放出气泡;可以和碱反应,不溶性碱能溶于酸;可以和盐反应,碳酸盐遇酸生成二氧化碳气体;
探究3:因为只要是碱性的溶液就能使无色酚酞变成红色,因为碳酸钠溶液显碱性,也会使无色酚酞变红色,所以不能仅仅根据溶液变红就判断制得了氢氧化钠,为了更具有说服力应该排除碳酸钠的干扰,即除去碳酸钠,根据碳酸钠的性质可以选用硝酸钡,氯化钡等溶液,然后过滤,在向滤液中加入酚酞根据溶液颜色的变红来判断.
故答案为:探究1:氧气;生成物含有氢元素和氧元素(反应前后元素种类不变);B;
探究2:
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中,加入锌粒(或加入氧化铜或加入氢氧化铜或加入碳酸钠等其它合理答案也可) | 有气泡产生(或出现蓝色溶液或固体溶解,溶液变蓝或有气泡产生等) | 证明研究结论正确 |
探究3:碳酸钠溶液也能使无色酚酞试液变红(或碳酸钠溶液也显碱性);
| 实验步骤 | 实验现象 | 实验结论 |
| 取少量样品于试管中,然后滴加适量的Ba(NO3)2溶液或加入足量的BaCl2溶液[或CaCl2)2溶液或Ca(NO3)2溶液…];过滤,在滤液中滴加几滴无色酚酞溶液. | 生成白色沉淀,酚酞溶液变红 | 无色溶液中确实 含有氢氧化钠 |
点评:探究物质的组成方法比较多,本题通过三种方法来验证物质的组成,同学们要根据实际情况进行应用,同时要熟练掌握酸碱盐的性质,知道碳酸钠虽然是盐,但是其溶液呈碱性.

练习册系列答案
 心算口算巧算一课一练系列答案
心算口算巧算一课一练系列答案 应用题作业本系列答案
应用题作业本系列答案
相关题目