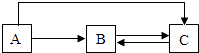题目内容
【题目】甲、乙两物质的溶解度曲线如图所示,下列说法错误的是( ) 
A.t1℃时,甲、乙两物质的溶解度相等
B.0~t1℃时,甲的溶解度小于乙的溶解度
C.t2℃时甲和乙的饱和溶液溶质质量分数大小关系:乙>甲
D.将甲的饱和溶液变为不饱和溶液,可采用升高温度的方法
【答案】C
【解析】解:A、据图可以看出,在t1℃时,甲、乙两物质的溶解度相等,正确; B、据图可以看出,0~t1℃时,甲的溶解度小于乙的溶解度,正确;
C、据图可以看出,在t2℃时甲的溶解度大于乙的溶解度,故甲和乙的饱和溶液溶质质量分数是甲的大于乙的,错误;
D、甲的溶解度随温度的升高而增大,故将甲的饱和溶液变为不饱和溶液,可采用升高温度的方法,正确;
故选C.
【考点精析】掌握饱和溶液和不饱和溶液相互转变的方法和固体溶解度曲线及其作用是解答本题的根本,需要知道饱和和不饱和的转变方法:①Ca(OH)2和气体等除外,它的溶解度随温度升高而降低②最可靠的方法是:加溶质、蒸发溶剂;1.查找指定温度时物质的溶解度,并根据溶解度判断溶解性.2.比较相同温度时(或一定温度范围内)不同物质溶解度的大小.3.比较和确定物质的溶解度受温度影响的程度,并据此确定物质结晶或混合物分离提纯的方法.4.确定溶液的状态(饱和与不饱和).

【题目】某化学兴趣小组在实验室制取O2时,取KClO3和MnO2的固体混合物若干克,加热至不再产生气体为止.他们通过加水测定剩余固体质量的方法来求出氧气的质量.实验结果如下表:(提示:MnO2是不溶于水的固体粉末)
实验序号 | 1 | 2 | 3 | 4 |
加水的质量(g) | 15 | 15 | 15 | 15 |
剩余固体的质量(g) | 14.1 | 9.3 | m | 4 |
请回答下列问题:
(1)KClO3的相对分子质量为;
(2)配平化学方程式:2KClO3 ![]() 2KCl+O2↑;
2KCl+O2↑;
(3)表中m值为;
(4)制得氧气的质量是多少?(写出计算过程)
【题目】用Ba(OH)2溶液测定某种氮肥中(NH4)2SO4的质量分数(杂质溶于水,但不参加反应).实验如下:称取该氮肥20g加水完全溶解,向该溶液中不断滴入Ba(OH)2溶液,生成气体及沉淀质量与加入Ba(OH)2溶液的质量关系如下所示: 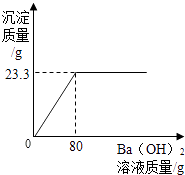
实验次序 | 1 | 2 | 3 |
滴入Ba(OH)2溶液的质量/g | 20 | 40 | 60 |
生成气体的质量/g | 0.85 | m | 2.55 |
试分析并计算:[已知:(NH4)2SO4+Ba(OH)2=BaSO4↓+2H2O+2NH3↑]
(1)表格中m的值为g.
(2)实验所用氢氧化钡溶液中溶质的质量分数.
(3)该氮肥中(NH4)2SO4的质量分数.(计算结果精确至0.1%)
【题目】下列四个图象能正确反映实验变化关系的有( )
A | B | C | D |
| |
|
|
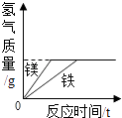
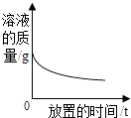
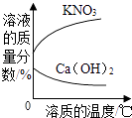
常温下,足量的镁、铁分别同时放入少量等质量、等质量分数的稀盐酸中 | 敞口放置于空气中的浓硫酸或稀盐酸 | 加热KNO3、Ca(OH)2的饱和溶液(不考虑溶剂的蒸发) | 少量的碳在密闭的集气瓶中与氧气完全燃烧 |
A.A
B.B
C.C
D.D