题目内容
某同学按照老师要求,配制20g 10%的氯化钠溶液,但是发现实验室没有纯净的氯化钠,只有含泥沙的粗盐.经过与同学的讨论,打算按如下步骤配制溶液: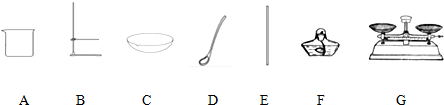
步骤一:粗盐提纯
(1)溶解:称取10g粗盐并加水溶解,需要用到如图中哪些仪器 .(填字母)
(2)过滤:在该操作中上图缺少的关键仪器是 .
(3)蒸发结晶:将滤液倒入蒸发皿中加热,当 可以停止加热.
步骤二:配制溶液
①计算:氯化钠的质量为 g,水为 ml.
②称量:用 称量氯化钠质量,用量筒来量取所需的水,量筒的规格是 (从下列中选用:10mL、20mL、50mL).量取液体时,量筒应放平稳,视线应与液体的 保持水平.
③溶解:把称取的氯化钠溶解在量取的水中,就能得到所需要的氯化钠溶液.

步骤一:粗盐提纯
(1)溶解:称取10g粗盐并加水溶解,需要用到如图中哪些仪器
(2)过滤:在该操作中上图缺少的关键仪器是
(3)蒸发结晶:将滤液倒入蒸发皿中加热,当
步骤二:配制溶液
①计算:氯化钠的质量为
②称量:用
③溶解:把称取的氯化钠溶解在量取的水中,就能得到所需要的氯化钠溶液.
考点:氯化钠与粗盐提纯,测量容器-量筒,一定溶质质量分数的溶液的配制,蒸发与蒸馏操作
专题:溶液、浊液与溶解度,常见的盐 化学肥料
分析:步骤一:粗盐提纯
(1)根据溶解需要用到烧杯和玻璃棒进行解答;
(2)根据过滤操作中上图缺少的关键仪器是漏斗进行解答;
(3)根据蒸发结晶:将滤液倒入蒸发皿中加热,当出现较多晶体时可以停止连续加热进行解答;
步骤二:配制溶液
①根据溶质质量分数公式分别求出氯化钠的质量和水的体积进行解答;
②根据用天平来称量氯化钠质量进行解答;根据选用量筒时,量程相近原则解答,根据量筒使用时正确读数的方法进行分析解答.
(1)根据溶解需要用到烧杯和玻璃棒进行解答;
(2)根据过滤操作中上图缺少的关键仪器是漏斗进行解答;
(3)根据蒸发结晶:将滤液倒入蒸发皿中加热,当出现较多晶体时可以停止连续加热进行解答;
步骤二:配制溶液
①根据溶质质量分数公式分别求出氯化钠的质量和水的体积进行解答;
②根据用天平来称量氯化钠质量进行解答;根据选用量筒时,量程相近原则解答,根据量筒使用时正确读数的方法进行分析解答.
解答:解:
步骤一:粗盐提纯
(1)溶解需要用到烧杯和玻璃棒;
(2)过滤操作中上图缺少的关键仪器是漏斗;
(3)蒸发结晶:将滤液倒入蒸发皿中加热,当出现较多晶体时可以停止连续加热;
步骤二:配制溶液
①需要氯化钠质量=20g×10%=2g,需要水的质量=20g-2g=18g,所以水的体积18mL;
②用天平来称量氯化钠质量;用量筒来量取所需的水,量筒的规格是20mL,用量筒量取液体体积时,正确读数的方法为:量筒必须放平,视线要与量筒内液体的凹液面的最低处保持水平;如果仰视则读数偏低,如果俯视则读数偏高.
答案:
步骤一:
(1)AE(2)漏斗(3)出现较多晶体时;
步骤二:
①2,18②天平 20mL 凹液面的最低处
步骤一:粗盐提纯
(1)溶解需要用到烧杯和玻璃棒;
(2)过滤操作中上图缺少的关键仪器是漏斗;
(3)蒸发结晶:将滤液倒入蒸发皿中加热,当出现较多晶体时可以停止连续加热;
步骤二:配制溶液
①需要氯化钠质量=20g×10%=2g,需要水的质量=20g-2g=18g,所以水的体积18mL;
②用天平来称量氯化钠质量;用量筒来量取所需的水,量筒的规格是20mL,用量筒量取液体体积时,正确读数的方法为:量筒必须放平,视线要与量筒内液体的凹液面的最低处保持水平;如果仰视则读数偏低,如果俯视则读数偏高.
答案:
步骤一:
(1)AE(2)漏斗(3)出现较多晶体时;
步骤二:
①2,18②天平 20mL 凹液面的最低处
点评:掌握溶解、过滤、蒸发等实验的操作技能;理解过滤法分离混合物的化学原理;体会过滤的原理在生活生产等社会实际中的应用.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
 目前,哈尔滨市有公交车辆5000余台,其中天然气公交车3000余台,CNG(压缩天然气)加气站共20余处.为满足哈市公交车辆天然气使用需求,2014年,哈市计划再建设4处加气站,让公交车用气更为方便.请根据信息回答问题:
目前,哈尔滨市有公交车辆5000余台,其中天然气公交车3000余台,CNG(压缩天然气)加气站共20余处.为满足哈市公交车辆天然气使用需求,2014年,哈市计划再建设4处加气站,让公交车用气更为方便.请根据信息回答问题:


 有四瓶标签破损的溶液,已知是碳酸钠、硫酸钠、一种含钠离子的溶液和一种硝酸盐.
有四瓶标签破损的溶液,已知是碳酸钠、硫酸钠、一种含钠离子的溶液和一种硝酸盐.