题目内容
【题目】从陶瓷、玻璃、水泥到电子芯片,硅元素的用途非常广泛。工业制取高纯硅的部分反应原理的微观示意图如下,有关说法不正确的是
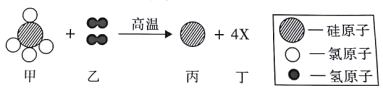
A. 该反应属于置换反应 B. X的化学式是HCl
C. 反应后硅元素的化合价升高 D. 图甲所示物质中硅、氯元素的质量比是14︰71
【答案】C
【解析】根据微观示意图可知,反应前的Si、H、Cl三种原子个数依次为1、4、4,反应后Si原子1个和4X,根据反应前后原子种类、数目均不变。4X含有H、Cl个数依次为4、4, X的化学式为HCl,该反应的化学方程式为:SiCl4+2H2![]() Si+4HCl。A、该反应是由一种单质和一种化合物反应,生成了一种化合物和一种单质,属于置换反应,正确;B、根据微观示意图可知,反应前的Si、H、Cl三种原子个数依次为1、4、4,反应后有Si原子1个和4X,根据反应前后原子种类、数目均不变。4X含有H、Cl个数为4、4, X的化学式为HCl ,正确;C、反应前的硅元素化合价为+4,生成物中硅元素均为0价,硅元素的化合价降低,错误; D、根据化学方程式可知,图甲所示物质中硅、氯元素的质量比是28:(35.5×4)=14:71,正确。故选C。
Si+4HCl。A、该反应是由一种单质和一种化合物反应,生成了一种化合物和一种单质,属于置换反应,正确;B、根据微观示意图可知,反应前的Si、H、Cl三种原子个数依次为1、4、4,反应后有Si原子1个和4X,根据反应前后原子种类、数目均不变。4X含有H、Cl个数为4、4, X的化学式为HCl ,正确;C、反应前的硅元素化合价为+4,生成物中硅元素均为0价,硅元素的化合价降低,错误; D、根据化学方程式可知,图甲所示物质中硅、氯元素的质量比是28:(35.5×4)=14:71,正确。故选C。

练习册系列答案
 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案
相关题目