题目内容
【题目】请根据下列装置图,回答有关问题:
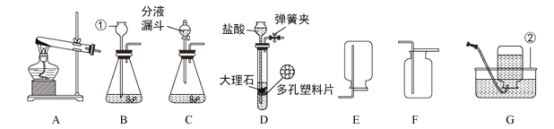
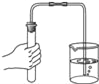
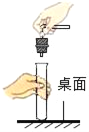
(1)写出图中标号仪器的名称:①______②______。
(2)实验室制取二氧化碳选择装置D作为发生装置的优点为_______对应选择的固体药品是____(填序号)。
A粉末状石灰石 B块状大理石 C粉末状生石灰 D块状生石灰
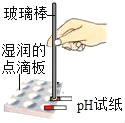
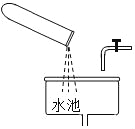
(3)实验室制取二氧化碳应该选用的收集装置是_____( 填序号) ,理由是_______检验二氧化碳是否收集满的操作方法是_______________。
(4)向含杂质的石灰石16g (杂质不与酸反应)加入足量稀盐酸,等溶液质量不再改变时测得生成二氧化碳3.36L (二氧化碳的密度约为1.96 g/L) ,则生成二氧化碳的质量为___________。(小数点后保留一位) 。求该石灰石样品的纯度__________________(请根据化学方程式进行计算,在答题纸写出计算过程)。
【答案】长颈漏斗 水槽 可以控制反应的发生和停止 B F 二氧化碳的密度比空气的密度大 将燃着的木条置于集气瓶口,若木条熄灭,则气体已收集满 6.6g 设该石灰石样品中碳酸钙的质量为x,则有:
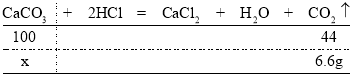
由![]() 解得x=15g
解得x=15g
则该石灰石样品的纯度为![]()
答:该石灰石样品的纯度为93.75%。
【解析】
(1)图中标号①仪器的名称为长颈漏斗,图中标号②仪器的名称为水槽。
(2)实验室制取二氧化碳选择装置D作为发生装置的优点为可以控制反应的发生和停止,对应选择的固体药品是块状大理石,B选项正确,符合题意。
(3)实验室制取二氧化碳应该选用的收集装置是向上排空气法,装置为F,理由是二氧化碳的密度比空气的密度大,检验二氧化碳是否收集满的操作方法是将燃着的木条置于集气瓶口,若木条熄灭,则气体已收集满。
(4)由题意生成二氧化碳的质量![]() 。设该石灰石样品中碳酸钙的质量为x,则有:
。设该石灰石样品中碳酸钙的质量为x,则有:

由![]() 解得x=15g
解得x=15g
则该石灰石样品的纯度为![]()
答:该石灰石样品的纯度为93.75%。

【题目】一定条件下,在密闭容器内投入SO2、O2、SO3、V2O5四种物质,发生反应的化学方程式为2SO2+O2![]() 2SO3。在不同时刻测得容器内各物质的质量如下表所示,下列说法不正确的是
2SO3。在不同时刻测得容器内各物质的质量如下表所示,下列说法不正确的是
物质 | 甲 | 乙 | 丙 | 丁 |
t1 | 80g | 5g | 100g | 5g |
t2 | a | 55g | 60g | b |
t3 | c | d | 40g | 5g |
A.甲是O2,丁是V2O5
B.a = 70g,d = 25g
C.参加反应的SO2、O2的分子个数比为2︰1
D.参加反应的SO2、O2的质量比为4︰1
【题目】在测定空气中氧气含量的实验中,小强采用了如图所示装置:在由两个注射器组成的密闭系统中留有![]() 空气,给装有细铜丝的玻璃管加热,同时交替缓慢推动两个注射器活塞,直到玻璃管内的铜丝在较长时间内无明显变化时停止加热,待冷却至室温后,将气体全部推至一个注射器内,观察密闭系统内气体体积的变化。
空气,给装有细铜丝的玻璃管加热,同时交替缓慢推动两个注射器活塞,直到玻璃管内的铜丝在较长时间内无明显变化时停止加热,待冷却至室温后,将气体全部推至一个注射器内,观察密闭系统内气体体积的变化。
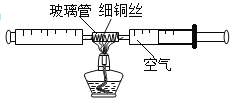
(1)在实验加热过程中,交替缓慢推动两个注射器活塞的目的是______。
(2)写出该实验中反应的文字表达式:______。
(3)小强测得的实验结果如下:
反应前注射器内气体总体积 | 反应后注射器内气体总体积 |
|
|
由此数据可以推算出他测定的空气中氧气的体积分数______(填“![]() ”、“
”、“![]() ”或“
”或“![]() ”)
”)![]() 。造成该实验出现误差的原因可能是______(填序号)。
。造成该实验出现误差的原因可能是______(填序号)。
①没有交替缓慢推动两个注射器活塞
②读数时没有冷却至室温
③加入铜丝量太少
④加入铜丝量太多
(4)通过上面的实验,你学到的测量混合物中某成分含量的方法是______。