题目内容
【题目】工业上,通过如下转化可制得KClO3晶体. 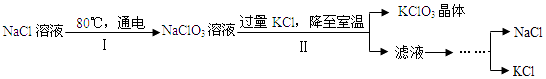
(1)KClO3中氯元素的化合价为 .
(2)生产中所用NaCl溶液由粗盐水精制而成,精制时除去粗盐水中泥沙,采用的操作是 .
(3)完善I中反应的化学方程式:NaCl+3H2O ![]() NaClO3+3 .
NaClO3+3 .
(4)已知NaC1O3+KCl=NaCl+KClO3 , Ⅱ中析出晶体后的滤液是KC1O3的(填“饱和溶液”或“不饱和溶液”).
(5)上述流程中,可循环利用的物质是 .
【答案】
(1)+5
(2)过滤
(3)H2↑
(4)饱和溶液
(5)NaCl、KCl
【解析】解:(1)设KClO3中氯元素的化合价为x, 根据题意有:(+1)+x+(﹣2)×3=0,
x=+5,
故填:+5.(2)生产中所用NaCl溶液由粗盐水精制而成,精制时除去粗盐水中泥沙,采用的操作是过滤.
故填:过滤.(3)由历史地理可知,I中反应的化学方程式为:NaCl+3H2O ![]() NaClO3+3H2↑.
NaClO3+3H2↑.
故填:H2↑.(4)Ⅱ中析出晶体后的滤液是KC1O3的饱和溶液,否则不能析出氯酸钾晶体.
故填:饱和溶液.(5)上述流程中,可循环利用的物质是NaCl、KCl.
故填:NaCl、KCl.
化合物中元素化合价代数和为零;
过滤可以把不溶于水的物质从溶液中分离出来;
化学反应前后元素种类不变,原子种类和总个数不变.

练习册系列答案
相关题目




