题目内容
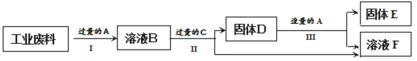
快手美食“自热米饭”中带有一个发热包,遇水后可迅速升温至150℃,保温时间达3小时,能将生米做成熟饭。某化学小组对发热包的固体成分进行了以下探究。
(查阅资料)
①发热包可能由生石灰、铁粉、镁粉、铝粉、炭粉、氯化钠中的若干种物质组成。
②MgCl2溶液、AlCl3溶液均能与NaOH溶液发生复分解反应生成白色沉淀。
③氢氧化镁不溶于NaOH溶液,氢氧化铝可溶于NaOH溶液。
(猜想1)固体中一定存在铁粉及生石灰
(实验1)
步骤 | 实验操作 | 实验现象 | 实验结论 |
1-1 | 取发热包内灰黑色的固体粉末,分成两份 | —— | —— |
1-2 | 用磁铁多次重复靠近其中一份粉末 | 有部分黑色固体被磁铁吸引 | _____ |
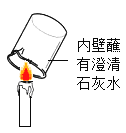
1-3 | 取另一份粉末于试管中,_____ | 放热,溶液变为红色 | 原粉末中一定含有生石灰 |
(猜想2)除上述物质外,还可能存在镁粉、铝粉和炭粉
(实验2)继续进行如下实验:
步骤 | 实验操作 | 实验现象 | 实验结论 |
2-1 | 取实验1-2的剩余固体于试管中,加入足量稀盐酸,充分反应后过滤 | _____,滤液呈无色 | 原粉末中一定含有炭粉,至少含镁粉、铝粉中的一种 |
2-2 | 取实验2-1的滤液于试管中,逐滴加入_____溶液至过量 | 先产生白色沉淀,后沉淀消失,变为无色溶液 |
(解释与结论)
(1)实验1-2的结论是_____。
(2)补全实验1-3的操作_____。
(3)补全实验2-1的现象_____。
(4)实验2-2加入的试剂是_____。
(反思与评价)
(5)根据上述实验可知,该发热包中一定不含有的物质是_____。
(6)氢氧化铝与NaOH反应生成偏铝酸钠(NaAlO2)和一种常见液态物质,该反应的化学方程式为_____。
请从A~C中任选两个作答,若均作答,按前两个计分。
序号 | A | B | C |
实验 装置 |
|
|
|
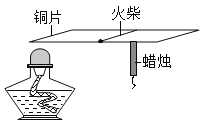
问题 | 该实验的目的是_____。 | 若用此实验成功验证质量守恒定律,改进的方法是_____。 | 能说明铜具有导热性的现象是_____。 |


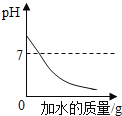 向NaOH溶液中加水稀释
向NaOH溶液中加水稀释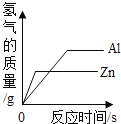 等质量的Al、Zn与足量的稀硫酸反应
等质量的Al、Zn与足量的稀硫酸反应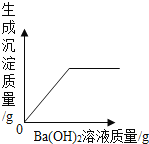 向稀硫酸中加入Ba(OH)2溶液
向稀硫酸中加入Ba(OH)2溶液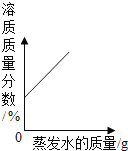 在恒温的条件下,适量蒸发饱和NaCl溶液的水分
在恒温的条件下,适量蒸发饱和NaCl溶液的水分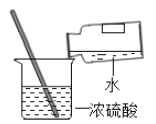 稀释浓硫酸 B.
稀释浓硫酸 B.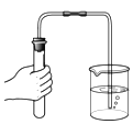 检查装置气密性
检查装置气密性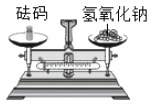 称量NaOH固体 D.
称量NaOH固体 D.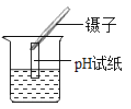 测定溶液的pH
测定溶液的pH