题目内容
【题目】从海水中得到的粗盐,往往含有可溶性杂质(主要有 Na2SO4、MgCl2、CaCl2)和不溶性杂质(泥沙等),必须进行分离和提纯后才能用于工业生产和人们的日常生活。粗盐提纯的部分流程如图:
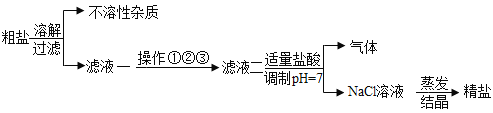
其中,滤液一至滤液二之间需进行三步操作:操作①:加入过量的碳酸钠,除去滤液中的Ca2+;操作②:加入过量的X,除去滤液中的Mg2+;操作③:加入过量的氯化钡,除去滤液中的SO42-。请回答:
(1)为最终获得精盐,操作①、②和③后还需增加的操作是_______;
(2)正确的操作顺序为_______(填序号);
(3)滤液二中加入适量稀盐酸的目的是______。
【答案】过滤 ②③① 除去过量的氢氧化钠和过量的碳酸钠
【解析】
(1)为最终获得精盐,操作①、②和③后还需增加的操作是过滤,将反应生成的沉淀除去;
(2)镁离子能和氢氧根离子结合成氢氧化镁沉淀,故可先加入过量的氢氧化钠,除去镁离子;然后加入过量的氯化钡,使钡离子与硫酸根离子结合成硫酸钡沉淀,除去硫酸根离子;再加入过量的碳酸钠,碳酸根离子和钙离子结合生成碳酸钙沉淀,除去钙离子,碳酸根离子和过量的钡离子结合生成碳酸钡沉淀,除去过量的钡离子。故正确的顺序是:②③①;
(3)因为稀盐酸与氢氧化钠反应生成氯化钠和水,稀盐酸与碳酸钠反应生成氯化钠、二氧化碳和水,所以滤液二中加入适量稀盐酸的目的是:除去过量的氢氧化钠和碳酸钠。

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目