题目内容
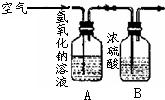 (2007?安徽)研究性学习小组选择从空气中制取氮气作为研究课题,以下是他们设计的实验
(2007?安徽)研究性学习小组选择从空气中制取氮气作为研究课题,以下是他们设计的实验方案:

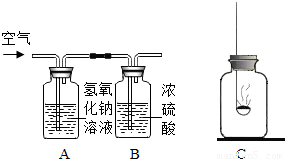
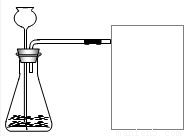
(1)除去二氧化碳和水蒸气:右图A装置中发生反应的化学方程式是
CO2+2NaOH=Na2CO3+H2O
CO2+2NaOH=Na2CO3+H2O
.B装置中浓硫酸的作用是
除去水蒸气
除去水蒸气
.
(2)除去氧气:他们分别收集一瓶气体用下图装置进行除去氧气的燃烧实验,其中甲同学选用红磷,乙同学选用木炭.你认为:选用
木炭
木炭
(填“红磷”或“木炭”)的方法不科学,原因是木炭燃烧产生二氧化碳气体,导致氮气不纯
木炭燃烧产生二氧化碳气体,导致氮气不纯
.(3)分析误差:此法得到的氮气密度(标准状况下)经科学测定,与氮气的实际密度有误差,请你分析出现误差的可能原因(只写两种,不考虑计算误差):①
稀有气体没有除去
稀有气体没有除去
;②氧气没有除尽
氧气没有除尽
.分析:(1)利用氢氧化钠可与二氧化碳反应、浓硫酸可吸收水的性质,达到除去二氧化碳和水蒸气实验目的;
(2)根据除去杂质的基本原则:不引入新的杂质,分析两种除去氧气方案的可行性,说明不可行方案不可行的理由;
(3)与氮气实际密度有误差,说明所得氮气不纯,试分析造成氮气不纯的原因.
(2)根据除去杂质的基本原则:不引入新的杂质,分析两种除去氧气方案的可行性,说明不可行方案不可行的理由;
(3)与氮气实际密度有误差,说明所得氮气不纯,试分析造成氮气不纯的原因.
解答:解:(1)利用装置A中的氢氧化钠溶液与二氧化碳反应生成碳酸钠和水而除去二氧化碳;利用浓硫酸的吸收性吸收气体中的水蒸气而除去水;
故选CO2+2NaOH=Na2CO3+H2O;除去水蒸气;
(2)由于木炭和氧气反应会生成气体二氧化碳,因此在除去氧气的同时又引入了新的气体杂质二氧化碳,所以乙同学方案不科学;
故答案为:木炭;木炭燃烧产生二氧化碳气体,导致氮气不纯;
(3)分析以上操作,会发现空气中的氧气、二氧化碳、水蒸气被除去,但空气中含量很少的稀有气体并没有除去,因此由于氮气中混有稀有气体而使氮气不纯,密度与实际密度有误差;
另外,在使用红磷除去氧气时,可能由于某种原因而没有把氧气完全除去而使所得氮气不纯,密度与实际密度有误差;
故答案为:稀有气体没有除去;氧气没有除尽.
故选CO2+2NaOH=Na2CO3+H2O;除去水蒸气;
(2)由于木炭和氧气反应会生成气体二氧化碳,因此在除去氧气的同时又引入了新的气体杂质二氧化碳,所以乙同学方案不科学;
故答案为:木炭;木炭燃烧产生二氧化碳气体,导致氮气不纯;
(3)分析以上操作,会发现空气中的氧气、二氧化碳、水蒸气被除去,但空气中含量很少的稀有气体并没有除去,因此由于氮气中混有稀有气体而使氮气不纯,密度与实际密度有误差;
另外,在使用红磷除去氧气时,可能由于某种原因而没有把氧气完全除去而使所得氮气不纯,密度与实际密度有误差;
故答案为:稀有气体没有除去;氧气没有除尽.
点评:选择气体除杂试剂的依据是:据气体的性质和要除去的杂质的性质.原则是:不能吸收要得到的气体,不能带入新的杂质.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案 导学与测试系列答案
导学与测试系列答案
相关题目
(2007?安徽)研究性学习小组选择“H2O2生成O2的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
假设:H2O2生成O2的快慢与催化剂种类有关
实验方案:常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一瓶(相同体积)O2所需的时间.
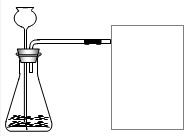
进行实验:下图是他们进行实验的装置图,气体发生装置中A仪器名称是,
此实验中B处宜采用的气体收集方法是.
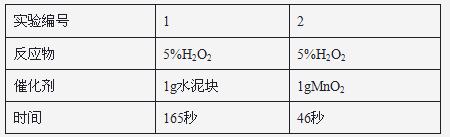
实验记录
结论:①该探究过程得出的结论是.
反思:②H2O2在常温下分解缓慢,加入MnO2或水泥块后反应明显加快,若要证明MnO2和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的,是否改变.
H2O2生成O2的快慢与哪些因素有关?请你帮助他们继续探究.(只要求提出一种影响H2O2生成O2的快慢的因素以及相关假设和实验方案)
假设:③.
实验方案:④
.
假设:H2O2生成O2的快慢与催化剂种类有关
实验方案:常温下,在两瓶同质量、同浓度的H2O2溶液中,分别加入相同质量的MnO2和水泥块,测量各生成一瓶(相同体积)O2所需的时间.
进行实验:下图是他们进行实验的装置图,气体发生装置中A仪器名称是,
此实验中B处宜采用的气体收集方法是.

实验记录
| 实验编号 | 1 | 2 |
| 反应物 | 5%H2O2 | 5%H2O2 |
| 催化剂 | 1g水泥块 | 1gMnO2 |
| 时间 | 165秒 | 46秒 |
反思:②H2O2在常温下分解缓慢,加入MnO2或水泥块后反应明显加快,若要证明MnO2和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的,是否改变.
H2O2生成O2的快慢与哪些因素有关?请你帮助他们继续探究.(只要求提出一种影响H2O2生成O2的快慢的因素以及相关假设和实验方案)
假设:③.
实验方案:④
.
 (2007?安徽)常温下,在两只各盛有100mL水的烧杯中,分别加入相同质量的甲、乙两种物质,使其充分溶解,结果如图所示.下列说法正确的是( )
(2007?安徽)常温下,在两只各盛有100mL水的烧杯中,分别加入相同质量的甲、乙两种物质,使其充分溶解,结果如图所示.下列说法正确的是( )