题目内容
【题目】下列关于燃烧现象的解释或分析正确的是

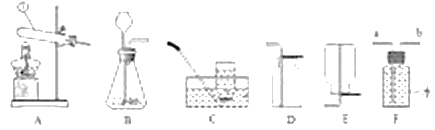
A.图a中将煤球变成蜂窝煤后再燃烧,其目的是延长煤燃烧的时间
B.图b中蜡烛火焰很快熄灭,是因为金属丝阻碍空气的流动
C.图c中的现象可知,金属镁燃烧的火灾不能用二氧化碳灭火
D.图d中火柴头斜向下时更容易燃烧,是因为降低了火柴梗的着火点
【答案】C
【解析】
A、煤做成蜂窝状,增大了煤与氧气的接触面积,能使煤充分燃烧,故A错误。
B、金属具有导热性,是热的良导体,当金属丝制成的线圈罩在蜡烛火焰上,金属丝由于吸热,致使燃烧产生的热量被快速传递,温度降到蜡烛的着火点以下,从而使蜡烛火焰熄灭,故B错误。
C、镁能在二氧化碳中燃烧,则金属镁燃烧的火灾不能用二氧化碳灭火,故C正确。
D、当火柴头斜向下时,燃烧产生的热量能给火柴梗预热,容易达到其着火点,所以更容易持续燃烧。而火柴头向上时,燃烧产生的热量随热空气上升,不能给火柴梗加热,火柴梗达不到其着火点,容易熄灭,故D错误。
故选C。

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
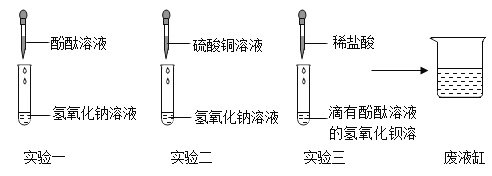
小博士期末闯关100分系列答案【题目】实验室里,区分下列各组物质的两个实验设计方案都合理的是![]()
序号 | A | B | C | D |
需区分的物质 | 生铁和钢 | 磷矿粉和碳铵 | 浓 | 氢氧化钠溶液和碳酸钠溶液 |
第一方案 | 分别取样,加入稀盐酸,观察现象 | 分别取样,加入试管中,闻气味 | 闻气味 | 分别取样,加入试管中,分别滴加无色酚酞溶液,观察现象 |
第二方案 | 分别用磁铁吸引,观察现象 | 分别取样,加入试管中,分别加入稀盐酸,观察现象 | 分别用玻璃棒蘸取少量试液,在白纸上写字,过一会观察现象 | 分别取样,加入试管中,分别滴加稀盐酸,观察现象 |
A.AB.BC.CD.D
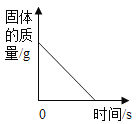
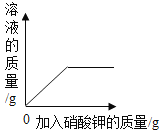
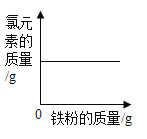
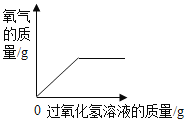
【题目】下列4个图像中,能正确反映对应变化关系的是
|
|
|
|
A.加热一定质量的高锰酸钾固体 | B.某温度下,向硝酸钾溶液中加入硝酸钾固体 | C.向一定质量的稀盐酸中加入铁粉 | D.向一定质量的二氧化锰中加入过氧化氢溶液 |
A.AB.BC.CD.D
【题目】NaCl是重要的工业原料,工业上可用电解饱和食盐水的方法获取烧碱、氯气、氢气等物质。实验小组的同学现欲对一份久置的工业烧碱的成分进行探究。
(查阅资料)电解饱和食盐水的化学方程式为:2NaCl+2H2O![]() 2NaOH+Cl2↑+H2↑。
2NaOH+Cl2↑+H2↑。
(提出问题)小组同学根据相关信息,对工业烧碱的成分作了如下猜想:
猜想一:NaOH、NaCl
猜想二:Na2CO3、NaCl
猜想三:_________________;
(实验探究)
为了验证猜想,小组同学进行了实验探究。首先取工业烧碱样品少许,配成溶液,待用。
(1)取样品溶液少许,滴加足量稀盐酸,有气泡产生,说明样品中含有________(填化学式),写出产生气泡的化学反应的方程式_________________;工业烧碱中含有该物质的原因是________(用化学方程式表示)。
(2)为了证明样品中含有NaCl,小组同学设计实验方案如下:先取样品溶液少量,向其中滴加足量的稀盐酸至不再产生气泡时,再向溶液中滴加AgNO3溶液,出现白色沉淀,加入稀硝酸后,沉淀不溶解,则样品中一定含有氯化钠。老师指出上述方案不合理,请说明理由_____;
(3)小组同学为进一步确认样品是否还含有氢氯化钠,设计了如下实验方案,请你将其补充完整。
实验操作步骤 | 实验现象 | 实验结论 |
①取样品溶液少许,加入足量氯化钙溶液,充分反应后静置 ②取反应后的溶液适量,滴加无色酚酞试液 | ①___________ ②____________ | 该样品中一定含有NaOH |
(反思与评价)
经过研究,小组同学认为,上述方案中,除了使用氯化钙以外,利用下列物质也可得到同样的效果,你认为下列哪些试剂是可行的_________(填序号)。
A Ca(OH)2 B Ca(NO3)2 C Ba(NO3)2 D Ba(OH)2
(数据处理)
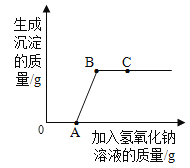
最终实验证实,该久置工业烧碱样品中含有氢氧化钠、氯化钠和碳酸钠。为了进一步确定该混合物中Na2CO3的质量分数,实验小组的同学取了10克该工业烧碱样品,加入足量的溶质质量分数为7.3%稀盐酸,实验测得生成CO2气体的质量与所加盐酸质量关系如图所示,请据图计算:
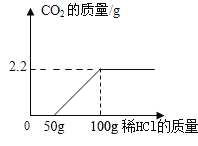
(1)该样品与稀盐酸完全反应时产生CO2的质量是____g。
(2)该样品中Na2CO3的质量分数____。