题目内容
【题目】某学生为了测定石灰石中碳酸钙的含量,取10g石灰石样品,经粉碎后放入烧杯中,并加入足量的稀盐酸使其反应(石灰石中的杂质不与酸发生反应),烧杯及所盛物质的总质量为80g,反应后烧杯及所盛物质的质量为77.8g,求:
(1)反应生成的二氧化碳气体为___________?
(2)该石灰石中碳酸钙的质量分数是_____________?
【答案】2.2g 50%
【解析】
根据质量守恒定律可知,过程中质量的减少是因为生成了二氧化碳,所以可以求算二氧化碳的质量,根据二氧化碳的质量和对应的化学方程式求算石灰石中碳酸钙的质量分数。
解:(1)根据质量守恒定律,二氧化碳的质量为:80g-77.8g=2.2g;
(2)设该石灰石样品中碳酸钙的质量分数为x,
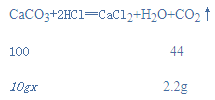
![]()
x=50%;
答:(1)反应生成的二氧化碳气体为2.2g;
(2)该石灰石中碳酸钙的质量分数是50%。

 小天才课时作业系列答案
小天才课时作业系列答案 一课四练系列答案
一课四练系列答案 黄冈小状元满分冲刺微测验系列答案
黄冈小状元满分冲刺微测验系列答案 新辅教导学系列答案
新辅教导学系列答案 阳光同学一线名师全优好卷系列答案
阳光同学一线名师全优好卷系列答案【题目】化学兴趣课上,同学们对过氧化钠(Na2O2)可以做供氧剂产生了浓厚兴趣,于是在老师的指导下展开了以下探究活动。
(提供资料)① 二氧化碳与过氧化钠反应生成氧气和另一种物质。
② 碳酸钠(Na2CO3)、碳酸氢钠(NaHCO3)与盐酸反应均能生成CO2。
③ 2Na2O2 + 2H2O= 4NaOH + O2↑。
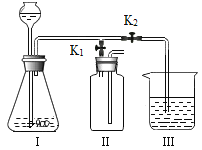
(1)证明二氧化碳与过氧化钠反应产生氧气并收集一瓶氧气。同学们在老师的指导下设计了如下图所示装置。
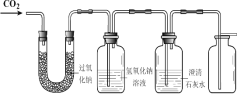
① 如何证明氧气已经收集满 ______。
② 氢氧化钠溶液的作用是除去未反应的二氧化碳,若观察到________ ,说明二氧化碳已经除尽。
(2)探究二氧化碳与过氧化钠反应生成的另一种物质。
(猜想与假设)下面是同学们提出的3种猜想。
猜想1:是氢氧化钠 猜想2:是碳酸氢钠 猜想3:是碳酸钠
通过对反应物中有关元素的组成分析,你认为猜想_____是不正确的,理由是____。
(进行实验)同学们通过以下实验验证了另一种物质,请完成下述实验报告。
实验操作 | 实验现象 | 实验结论 |
取少量CO2与Na2O2反应后的固体于试管中,___________。 | 有大量气泡产生,澄清石灰水变浑浊。 | 猜想_____ 是正确的。 |
(反思与评价)若用人呼出的气体通过上图装置,证明二氧化碳与过氧化钠反应生成了氧气,你是否同意这种做法,并阐述理由____ 。