��Ŀ����
�ס��ҡ�A��B��C��D�dz��л�ѧ�������ʣ�����A��B��C��D����H��C��O��Ca��NaԪ���е����ֻ�������ɣ�
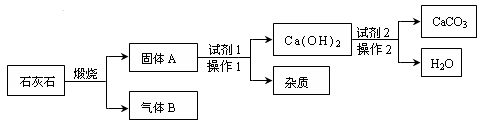
��1������θ�����Ҫ�ɷ֣�����ý�����Ӧ����һ���ڱ�״�����ܶ���С�����壬�����廯ѧʽΪ������
��2������һ�ֺ�ɫ�������������ϡ���ᣬ�õ���ɫ��Һ�����ҵĻ�ѧʽΪ�� ����
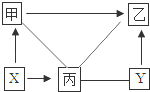
��3��A�׳�Ϊ���B��C��D���������к�ͬ�ֽ���Ԫ�أ�����������ת����ϵB��C��D��A��C��Ӧ�Ļ�ѧ����ʽΪ�� ����
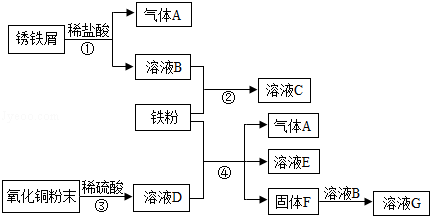
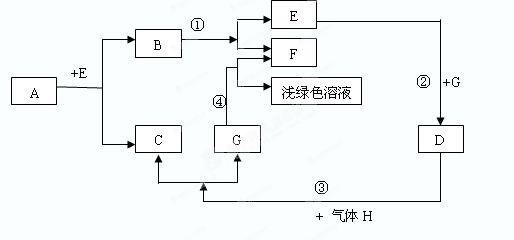
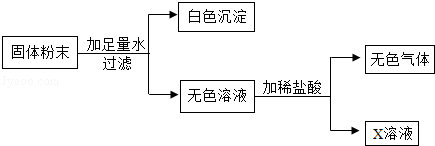
��4��ʵ��С��ͬѧ��A��B��C��D�е�һ�ֻ������ʻ����һ��õ�һ����ɫ�����ĩ��Ϊȷ������ɣ�����������ͼ��ʾ��ʵ�飮
��ش�
����X��Һֻ��һ�����ʣ�����ʵ�����ȷ��X��Һ�е��������� ����
�����жԹ����ĩ�ɷֵ��ж��У�����ȷ������ ��������ĸ��ţ���
A��һ����̼����
B��һ����̼���
C�������������ơ��������ơ�̼��ƵĻ����
D���ù����ĩ�������������������
��1������θ�����Ҫ�ɷ֣�����ý�����Ӧ����һ���ڱ�״�����ܶ���С�����壬�����廯ѧʽΪ������
��2������һ�ֺ�ɫ�������������ϡ���ᣬ�õ���ɫ��Һ�����ҵĻ�ѧʽΪ�� ����
��3��A�׳�Ϊ���B��C��D���������к�ͬ�ֽ���Ԫ�أ�����������ת����ϵB��C��D��A��C��Ӧ�Ļ�ѧ����ʽΪ�� ����
��4��ʵ��С��ͬѧ��A��B��C��D�е�һ�ֻ������ʻ����һ��õ�һ����ɫ�����ĩ��Ϊȷ������ɣ�����������ͼ��ʾ��ʵ�飮

��ش�
����X��Һֻ��һ�����ʣ�����ʵ�����ȷ��X��Һ�е��������� ����
�����жԹ����ĩ�ɷֵ��ж��У�����ȷ������ ��������ĸ��ţ���
A��һ����̼����
B��һ����̼���
C�������������ơ��������ơ�̼��ƵĻ����
D���ù����ĩ�������������������
��1��H2 ��2��Fe2O3��3��Ca��OH��2+Na2CO3=CaCO3��+2NaOH��4����NaCl ��BCD
�����������1������θ�����Ҫ�ɷ֣����Ϊ���ᣬ��������ý�����Ӧ�����������ʸ����廯ѧʽΪ H2����2����ɫ��Һ�к��������ӣ���ɫ��������Ϊ����������ϡ���ᷴӦ�����Ȼ�����ˮ������Ϊ����������ѧʽΪ Fe2O3����3��A�׳�Ϊ�����AΪ̼���ƣ�B��C��D���������к�ͬ�ֽ���Ԫ�أ����������ж����и����ӣ��������ʼ�������ת����ϵB��C��D����BΪ�����ƣ�CΪ�������ƣ�DΪ̼��ƣ���������ˮ��Ӧ�����������ƣ����������������̼��Ӧ����̼��ƣ���A��C�ķ�ӦΪ̼������������������̼��ƺ��������ƣ���ѧ����ʽΪ Ca��OH��2+Na2CO3=CaCO3��+2NaO��4����������������֪AΪ̼���ƣ�BΪ�����ƣ�CΪ�������ƣ�DΪ̼��ƣ������ĩ�м�������ˮ������ɫ��������ɫ��Һ����ɫ��Һ�м����������ɫ���壬����Һ��һ������̼���ƣ�̼���������ᷴӦ�����Ȼ��ƣ���X��Һֻ��һ�����ʣ��������һ�����Ȼ��ƣ���������ʵ����ɫ��Һ�м����������ɫ���壬����Һ��һ������̼���ƣ�̼���������ᷴӦ����������̼����A˵����ȷ�������ĩ�м�������ˮ������ɫ�������˰�ɫ����������ԭ��ĩ�к��е�̼��ƣ�Ҳ������̼�������������Ʒ�Ӧ���ɵ�̼��ƣ���������δ�ܽ���������ƣ���˲�һ������̼��ƣ�B˵�����÷�ĩ��һ������̼���ƣ���C˵��������ʵ��ֻ�ܵ�֪�÷�ĩ��һ������̼���ƣ��������ʶ�����ȷ������˸÷�ĩ����ɳɷֿ����������������̼���ƺ������ƣ���̼�������������Ƣ�̼������̼��Ƣ�̼���ơ����������������Ƣ�̼���ơ������ƺ�̼��Ƣ�̼���ơ��������ƺ�̼��Ƣ�̼���ơ������ơ��������ƺ�̼��ƹ������������D˵������ѡBCD

��ϰ��ϵ�д�
 �Ͻ�ƽ��У����ϵ�д�
�Ͻ�ƽ��У����ϵ�д�
�����Ŀ