题目内容
【题目】食盐是一种重要的化工原料。请回答下列问题。
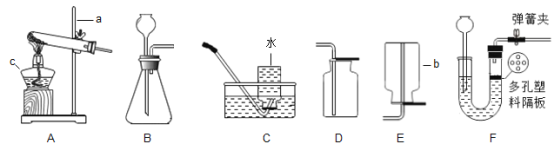
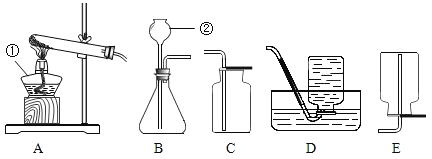
(1)由于粗盐中含有少量MgCl2、CaCl2、Na2SO4等杂质,不能满足化工生产的要求,因此必须将粗盐进行精制。流程如下图。

①加入稍过量的Na2CO3溶液除了能除去粗盐中的CaCl2外,它还有一个作用是_____。
②操作Ⅲ的名称_____,所用的玻璃仪器有:烧杯、玻璃棒和_____。
③在蒸发过程中,待_____时,停止加热,利用余热将滤液蒸干。
(2)若有溶质质量分数为10%的氯化钠不饱和溶液100 kg,要将其变成20 ℃时氯化钠的饱和溶液,以满足化工生产的需要,可采用的最简便方法是_____。已知:20 ℃时氯化钠的溶解度为36g。
【答案】除去过量的BaCl2 过滤 漏斗 蒸发皿中出现较多固体时 加入22.4kg氯化钠固体
【解析】
(1)①碳酸钠和氯化钡反应生成碳酸钡沉淀和氯化钠,碳酸钠和氯化钙反应生成碳酸钙沉淀和氯化钠,加入稍过量的Na2CO3溶液除了能除去粗盐中的CaCl2外,它还有一个作用是除去过量的BaCl2;
②操作Ⅲ能将固体与液体分离,其名称过滤,所用的玻璃仪器有:烧杯、玻璃棒和漏斗;
③在蒸发过程中,为防止固体溅出,待蒸发皿中出现较多固体时时,停止加热,利用余热将滤液蒸干;
(2)20℃时氯化钠的溶解度为36g,可以通过加入氯化钠固体的方法是溶液达到饱和状态,设需要加入氯化钠为x,
![]() x=22.4kg。要将其变成20 ℃时氯化钠的饱和溶液,以满足化工生产的需要,可采用的最简便方法是加入22.4kg氯化钠固体。
x=22.4kg。要将其变成20 ℃时氯化钠的饱和溶液,以满足化工生产的需要,可采用的最简便方法是加入22.4kg氯化钠固体。

 津桥教育计算小状元系列答案
津桥教育计算小状元系列答案【题目】按下表进行试验,在等质量的大理石中加入足量的酸(假设杂质不与酸反应),用数字检测仪分别测得产生的二氧化碳体积随时间的变化曲线如图所示。根据图示,下列说法正确的是
实验编号 | 药 品 |
Ⅰ | 块状大理石、10%的稀硫酸溶液 |
Ⅱ | 块状大理石、7%的稀盐酸溶液 |
Ⅲ | 粉末状大理石、7%的稀盐酸溶液 |
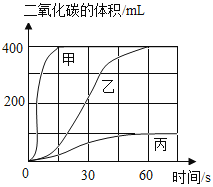
A.曲线甲代表的是实验I
B.实验室可用块状大理石和10%的稀硫酸溶液反应制取二氧化碳
C.实验室可用粉末状大理石和7%的稀盐酸溶液反应制取二氧化碳
D.据图分析,在其他条件相同时,固体的颗粒越小,反应速率越快
【题目】某同学为了测定铜镁混合物中铜的质量分数,将100g稀盐酸分2次加入到盛有5g该固体混合物的烧杯中,所得数据如下表。(提示:铜镁混合物中的镁能和稀盐酸反应生成氯化镁和氢气,而铜不与稀盐酸反应、也不溶于水)则下列说法中错误的是( )
次数 | 实验前 | 第1次 | 第2次 |
加入稀盐酸的质量/g | 0 | 50 | 50 |
剩余固体的质量/g | 5 | 3 | 2 |
A.第1次加入稀盐酸后剩余固体中还有镁
B.第2次所加入的稀盐酸未反应完
C.每50g稀盐酸和1g镁恰好能完全反应
D.原混合物中铜的质量分数为40%