题目内容
【题目】请根据下列装置回答问题:

(1)写出标号仪器名称:a___.
(2)在A装置中加入高锰酸钾制备氧气的化学方程式是___.
(3)实验室制取二氧化碳的化学方程式为___,其发生装置是___(填序号)若要收集干燥的CO2则需要在装置F中加入___(填物质名称)将气体通过后F再用___(在A~E中选择)装置收集气体.
(4)赵斌钰同学想验证CO2的性质,他将B、F装置连接,在F装置中加入澄清石灰水在B装置中加入足量浓盐酸与石灰石,结果发现石灰水不浑浊,原因是___(装置气密性良好,试剂未变质).
【答案】水槽 2KMnO4![]() K2MnO4+MnO2+O2↑ CaCO3+2HCl═CaCl2+CO2↑+H2O B 浓硫酸 C 浓盐酸具有挥发性,氯化氢溶于水就是盐酸,会消耗掉氢氧化钙
K2MnO4+MnO2+O2↑ CaCO3+2HCl═CaCl2+CO2↑+H2O B 浓硫酸 C 浓盐酸具有挥发性,氯化氢溶于水就是盐酸,会消耗掉氢氧化钙
【解析】
(1)标号仪器是水槽;故填:水槽
(2)高锰酸钾在加热的条件下可以分解产生二氧化锰、锰酸钾和氧气,化学方程式为:2KMnO4![]() K2MnO4+MnO2+O2↑,该反应需要加热,故发生装置应是“固体加热型”,故选A
K2MnO4+MnO2+O2↑,该反应需要加热,故发生装置应是“固体加热型”,故选A
(3)实验室中制取二氧化碳常用大理石和稀盐酸反应来制取,属于隔夜常温型,故选B,化学方程式为:CaCO3+2HCl═CaCl2+CO2↑+H2O;浓硫酸具有吸水性,若要收集干燥的CO2则需要在装置F中加入浓硫酸;二氧化碳密度比空气大,能够溶于水,所以应该选择C装置来收集二氧化碳;故填:B;CaCO3+2HCl═CaCl2+CO2↑+H2O;浓硫酸;C
(4)因为浓盐酸具有挥发性,所以浓盐酸和石灰石制取的二氧化碳中含有氯化氢气体,氯化氢溶于水就是盐酸,会消耗掉氢氧化钙,所以发现澄清石灰水不浑浊。故填:浓盐酸具有挥发性,氯化氢溶于水就是盐酸,会消耗掉氢氧化钙

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案【题目】依据下列实验和数据回答下列问题。
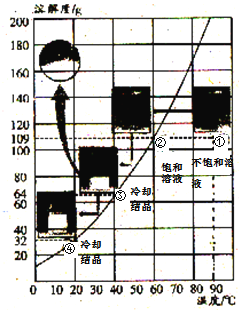
在下表对应的温度下,向4只盛有100 g水的烧杯中,分别加入40 g KCl固体,充分溶解。KCl的溶解度曲线如图。

烧杯序号 | ① | ② | ③ | ④ |
温度(℃) | 20 | 30 | 50 | 60 |
【1】①~④所得溶液属于饱和溶液的是()
A. ①② B. ②③ C. ③④ D. ①④
【2】下列关于①~④所得溶液的说法不正确的是()
A. 溶质质量 ①<② B. 溶液质量 ②<③
C. 溶质质量分数 ③<④ D. ④中溶质与溶剂的质量比为 2:5