题目内容
【题目】研究“水”可从多角度展开。
(1)水的电解
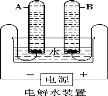
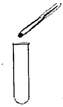
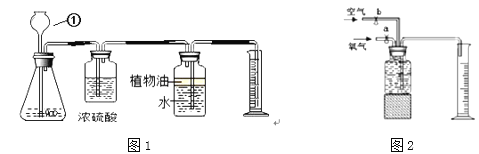
①宏观现象:按如图所示装置,通电一段时间后,试管A、B中产生气体的体积比约为__________,检验B中气体时的现象是__________。
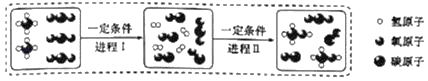
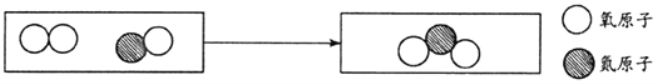
②微观该反应中发生分解的微粒名称是__________。
③结论:水由__________组成。
(2)水的性质
将黄豆大小的金属钠放入盛有水的烧杯中,生成氢氧化钠和一种密度最小的气体;写出该反应的化学方程式__________。
(3)水的用途
①碘与锌在常温下反应速度很慢,若滴入几滴水则反应剧烈,水在此处的作用是__________。
②下列实验中,对水的主要作用分析不够全面的是__________(填字母)
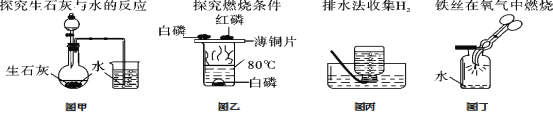
A.图甲中的水便于观察烧瓶内气压变化
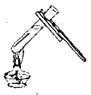
B.图乙中的水提供热量
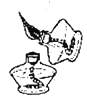
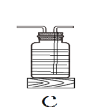
C.图丙集气瓶中的水排尽空气且便于观察H2何时集满
D.图丁中的水防止熔融物炸裂集气瓶
【答案】2∶1 带火星的木条复燃 水分子 氢氧元素(或H、O) 2Na+2H2O=2NaOH+H2↑ 加快反应速度(或催化剂) AB
【解析】
(1)①图1是电解水的实验,玻璃管A、B中产生气体的体积分别是电源的负极、正极分别生成的氢气和氧气,体积比约为2:1,B中的气体是氧气具有助燃性,检验B中气体的现象是:打开活塞,带火星的木条靠近管口,木条复燃;
②化学变化中,分子离解成原子,原子重新结合成新的微粒。该反应中发生分解的微粒名称是水分子;
③电解水生成了氢气和氧气,氢气是由氢元素组成,氧气是由氧元素组成,化学变化中元素的种类不变,说明了水由氢、氧元素(或H、O)组成的;
(2)将黄豆大小的金属钠放入盛有水的烧杯中,生成氢氧化钠和一种密度最小的气体,密度最小的气体是氢气。该反应的化学方程式为:2Na+2H2O=2NaOH+H2↑;
(3)①碘与镁在常温下化合速度很慢,若滴入几滴水则反应剧烈,水在此处的作用是加快反应速度(或催化剂);
②A、氧化钙与水化合生成了氢氧化钙放出了大量的热,烧瓶内温度升高压强增大,导管口有气泡生成,烧杯中的水便于观察烧瓶内气压变化,烧瓶内的水是用作反应物,故A错误;
B、在探究燃烧的条件时,水的作用是能提供热量和隔绝空气的作用,故B错误;
C、利用排水法收集氢气时,排尽空气且便于观察H2何时集满,故C正确;
D、铁丝在氧气中燃烧时,集气瓶中的水:冷却溅落融熔物,防止集气瓶炸裂,故D正确。故选AB。

 星级口算天天练系列答案
星级口算天天练系列答案 芒果教辅达标测试卷系列答案
芒果教辅达标测试卷系列答案