题目内容
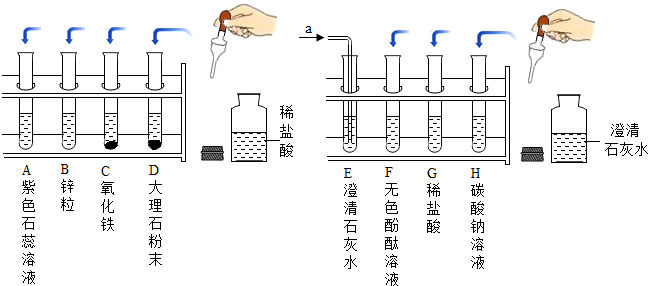
某化学实验小组探究稀盐酸、氢氧化钙两种物质的化学性质,取8支试管分别用A~H编号后,进行如图所示实验请回答: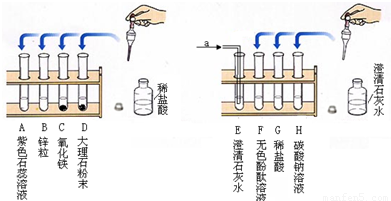
(1)实验中,有气泡产生的试管是 (填试管标号);实验中,无明显现象的试管是 (填试管标号).
(2)实验后某试管中为红色溶液,当向其中加入过量的 后,溶液变为蓝色.则该试管中最初盛有的物质是 .
(3)写出试管C中反应的化学方程式: .
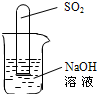
(4)实验中,观察到试管E中澄清石灰水变浑浊,则气体a是 .
(5)写出试管H中反应的化学方程式: ;
从复分解反应的条件考虑,这一反应能发生的理由是 .
【答案】分析:(1)酸与金属反应生成盐和氢气,酸与碳酸盐反应生成盐、水、二氧化碳;根据反应后产物中有沉淀生成的实验考虑;无明显现象是指没有沉淀生成,没有气体放出,没有颜色变化的反应;
(2)由红色变为蓝色是紫色石蕊试液遇到酸和碱呈现的不同现象;
(3)氧化铁和稀盐酸反应生成氯化铁和水,写出反应的方程式;
(4)二氧化碳能使澄清的石灰水变浑浊;
(5)氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,写出反应的方程式;根据复分解反应的条件分析.
解答:解;(1)铁与盐酸反应生成氯化亚铁和氢气;碳酸钠与盐酸反应生成氯化钠、水、二氧化碳,所以有气泡出现的试管是BD;氢氧化钙与盐酸反应的生成物是氯化钙和水,故反应过程中无明显现象是G;
(2)在A试管中盛有紫色石蕊试液,加入盐酸后,显酸性,酸能使紫色石蕊试液变红色,再向其中加入氢氧化钠等碱性溶液,当氢氧化钠等把盐酸反应掉后,显碱性时,碱能使紫色石蕊试液变蓝色;
(3)氧化铁和稀盐酸反应生成氯化铁和水,反应的方程式为:Fe2O3+6HCl=2FeCl3+3H2O;
(4)二氧化碳能使澄清的石灰水变浑浊,因此实验中,观察到试管E中澄清石灰水变浑浊,则气体a是可能是二氧化碳;
(5)氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,反应的方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;该反应有沉淀产生,符合复分解反应发生的条件;
故答案为;(1)BD;G;(2)澄清石灰水(或氢氧化钠溶液等);紫色石蕊试液;(3)Fe2O3+6HCl=2FeCl3+3H2O;(4)二氧化碳;(5)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;生成沉淀(或有沉淀生成).
点评:本题主要考查了酸碱的化学性质以及二氧化碳气体的检验等知识,难度不大,解答时抓住酸和碱的化学性质及发生的反应即可解答.
(2)由红色变为蓝色是紫色石蕊试液遇到酸和碱呈现的不同现象;
(3)氧化铁和稀盐酸反应生成氯化铁和水,写出反应的方程式;
(4)二氧化碳能使澄清的石灰水变浑浊;
(5)氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,写出反应的方程式;根据复分解反应的条件分析.
解答:解;(1)铁与盐酸反应生成氯化亚铁和氢气;碳酸钠与盐酸反应生成氯化钠、水、二氧化碳,所以有气泡出现的试管是BD;氢氧化钙与盐酸反应的生成物是氯化钙和水,故反应过程中无明显现象是G;
(2)在A试管中盛有紫色石蕊试液,加入盐酸后,显酸性,酸能使紫色石蕊试液变红色,再向其中加入氢氧化钠等碱性溶液,当氢氧化钠等把盐酸反应掉后,显碱性时,碱能使紫色石蕊试液变蓝色;
(3)氧化铁和稀盐酸反应生成氯化铁和水,反应的方程式为:Fe2O3+6HCl=2FeCl3+3H2O;
(4)二氧化碳能使澄清的石灰水变浑浊,因此实验中,观察到试管E中澄清石灰水变浑浊,则气体a是可能是二氧化碳;
(5)氢氧化钙和碳酸钠反应生成碳酸钙和氢氧化钠,反应的方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;该反应有沉淀产生,符合复分解反应发生的条件;
故答案为;(1)BD;G;(2)澄清石灰水(或氢氧化钠溶液等);紫色石蕊试液;(3)Fe2O3+6HCl=2FeCl3+3H2O;(4)二氧化碳;(5)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH;生成沉淀(或有沉淀生成).
点评:本题主要考查了酸碱的化学性质以及二氧化碳气体的检验等知识,难度不大,解答时抓住酸和碱的化学性质及发生的反应即可解答.

练习册系列答案
相关题目
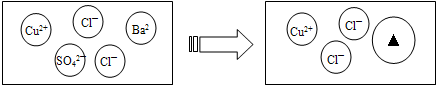
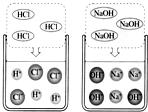 24、某化学兴趣小组利用“稀盐酸、硫酸铜、氢氧化钠、氯化钡”几种物质对复分解反应进行再探究.
24、某化学兴趣小组利用“稀盐酸、硫酸铜、氢氧化钠、氯化钡”几种物质对复分解反应进行再探究.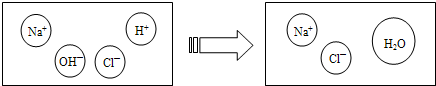
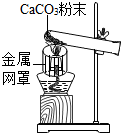 某化学实验小组在实验室用下图装置做CaCO3受热分解的实验.加热一段时间后,同学们对试管内剩余固体的成分进行探究.请你参与探究.
某化学实验小组在实验室用下图装置做CaCO3受热分解的实验.加热一段时间后,同学们对试管内剩余固体的成分进行探究.请你参与探究.