题目内容
【题目】海水是一种重要资源,从海水中可提取食盐、MgCl2等多种物质.
(1)从海水中提取粗盐一般采用的方法.
(2)海水提取粗盐后得到卤水,卤水中主要成分的溶解度与温度的关系如图所示. ①t2℃时,MgCl2的溶解度是 , 此温度下 MgCl2饱和 溶液中溶质与溶剂的质量比是 .
②t1℃时,三种物质中溶解度最小的是 .
③将 t2℃时 MgSO4的饱和溶液降温至 t1℃,得到 MgSO4的溶液(填“饱和”或“不饱和”),原因是 . 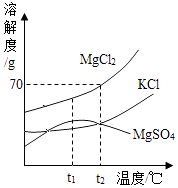
【答案】
(1)蒸发溶剂
(2)70g;7:10;氯化钾;不饱和;t1℃时MgSO4的溶解度大于t2℃时MgSO4的溶解度
【解析】解:(1)从海水中提取粗盐一般采用蒸发结晶的方法;(2)①通过分析溶解度曲线可知,t2℃时,MgCl2的溶解度是70g,此温度下MgCl2饱和溶液中溶质与溶剂的质量比是70g:100g=7:10;②t1℃时,三种物质中溶解度最小的是KCl;③将t2℃时MgSO4的饱和溶液降温至t1℃,得到MgSO4的不饱和溶液,因为t1℃时MgSO4的溶解度大于t2℃时MgSO4的溶解度.故答案为:(1)蒸发结晶;(2)①70g,7:10;②KCl;③不饱和,t1℃时MgSO4的溶解度大于t2℃时MgSO4的溶解度. 根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的.

练习册系列答案
相关题目