题目内容
【题目】取12.4g碳酸铜(CuCO3,式量124)粉末放入盛有92g稀硫酸的烧杯中,恰好完全反应,生产的CO2气体全部逸出。请计算:
(1)反应生产H2O的质量。
(2)反应后烧杯中硫酸铜(式量160)溶液溶质的质量分数。
【答案】
【解析】分析:碳酸铜和硫酸反应,生成硫酸铜、水和二氧化碳,两物质恰好完全反应时,所得溶液为硫酸铜溶液;
根据反应的化学方程式,利用参加反应的碳酸铜的质量,可计算反应中生成水的质量、反应生成硫酸铜的质量;
反应后烧杯中硫酸铜溶液溶质的质量分数=![]() ×100%,反应后溶液质量可利用质量守恒定律求得.
×100%,反应后溶液质量可利用质量守恒定律求得.
解:设反应生成水的质量为x,生成硫酸铜的质量为y,生成气体二氧化碳的质量为z
CuCO3+H2SO4=CuSO4+CO2↑+H2O
124 160 44 18
12.4g y z x
![]()
x=1.8g
![]()
![]()
![]() z=4.4g
z=4.4g
反应后硫酸铜溶液质量=12.4g+92g-4.4g=100.0g
硫酸铜溶液的溶质质量分数=![]() ×100%=16%
×100%=16%
答:(1)反应生产H2O的质量为1.8g;
(2)反应后烧杯中硫酸铜(式量160)溶液溶质的质量分数为16%.

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】某化学实验小组对“影响石灰石与盐酸反应速率的因素﹣﹣盐酸的浓度和石灰石的颗粒大小等”进行了如下实验探究,请你参与.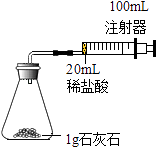
[进行实验]
室温下,选用20mL不同溶质质量分数的盐酸(4%和6%)分别与1g颗粒状或块状的石灰石进行实验(固定夹持仪器略去).
(1)石灰石与盐酸反应的化学方程式为 .
(2)按上图装置进行实验,在装药品前应检查该装置的气密性,具体的做法是 . 开始实验时,应将20mL稀盐酸(选填“快速”或“缓慢”)推入锥形瓶中,以保证盐酸能全部推入锥形瓶中.
(3)[处理数据]
实验小组进行实验后,获得的相关实验数据如表所示:
实验编号 | 盐酸溶质质量分数 | 石灰石固体形状 | 二氧化碳体积(mL) |
a | 4% | 颗粒 | 64.0 |
b | 4% | 块状 | 40.4 |
c | 6% | 颗粒 | 98.2 |
d | 6% | 块状 | 65.3 |
①要比较(写一组),由此可得到的结论是 .
②从上述实验中得出石灰石的颗粒大小反应速率影响的结论是 .
(4)[拓展延伸]
如表是实验时记录生成的二氧化碳气体体积和对应的时间的一组实验数据(每间隔4S读数一次):
时间/S | 4 | 8 | 12 | 16 | 20 | 24 | 28 | 32 | 36 | 40 |
气体体积/mL | 16.0 | 22.2 | 29.4 | 39.3 | 50.4 | 57.6 | 62.0 | 64.7 | 66.0 | 66.0 |
从上表数据可以分析得出,到20S后反应速率逐渐变 , 其主要原因是 .
(5)你认为影响石灰石与盐酸反应速率的因素还有 , 请设计实验方案验证你的猜想