��Ŀ����
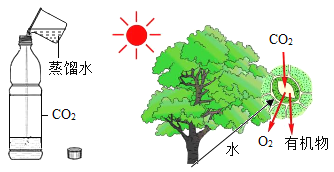
����Ŀ��ѧϰ�˵��ʡ�������ᡢ��ε����ʺ����кܶͬ���������ڷ�����Ӧʱ����������(��������ʡ��)����ͼ��ʾ����ش�
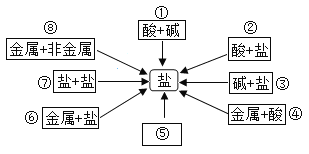
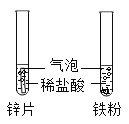
(1) ����������أ�����з�����Ӧ�Ļ�ѧ����ʽ________��
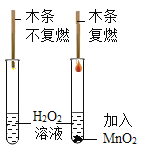
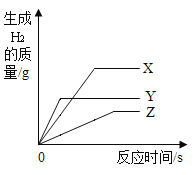
(2)�������Ȼ���������������ʾ�ı仯�п���ͨ���û���Ӧ��ʵ�ֵ���_____(�����)��
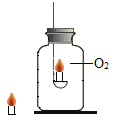
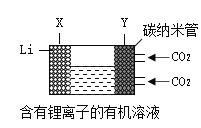
(3)�����ܹ�������Ӧ������������У�_______��
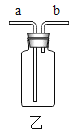
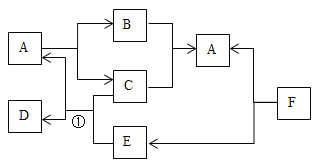
(4)ͼ�Тݴ�Ӧ�����������_______(дһ�֣�������ͼ��������Ϣ�ظ�)��
���𰸡�2KOH+H2SO4=K2SO4+2H2O �ܢ� �������г����������ˮ���� ��+����������
��������
��1������������أ����з����ķ�Ӧ���������غ����ᷴӦ��������غ�ˮ����ѧ����ʽΪ��2KOH+H2SO4=K2SO4+2H2O��
��2���������Ȼ�������������ʾ�ı仯�п���ͨ���û���Ӧ��ʵ�ֵ��У��������ᷴӦ�������Ȼ������������Ȼ�ͭ�������Ȼ�����������������������������Ȼ���������ѡ�ܢޣ�
��3�������κ��ᷴӦ������������Σ����ڸ��ֽⷴӦ�����ݸ��ֽⷴӦ��������֪���������г����������ˮ���ɷ�Ӧ���ܷ�����
��4��������е�ת����ϵ��ͼ�Тݴ�Ӧ����������ǣ���+���������

����Ŀ��ʵ��������һƿ���õ���ɫҺ���Լ����ܲ�����ɱ�ǩ����(��ͼ��ʾ)�����ȱ�ı�ǩ��ֻʣ����Na������10%��������Сǿ��С��ͬѧ�Դ˺���Ȥ����������ɷֽ���̽����
��������⣩��ƿ�Լ�������ʲô���ʵ���Һ�أ�
���������ϣ�I�����л�ѧ�г����ĺ��ƻ������У�NaCl��NaOH��Na2CO3��NaHCO3��
II��Na2CO3��NaHCO3��ˮ��Һ���ʼ��ԡ�
�ⶨ����(20C)ʱ���������ʵ��ܽ���������£�
���� | NaCl | NaOH | Na2CO3 | NaHCO3 |
�ܽ��/g | 36 | 109 | 205 | 9.6 |
���ó����ۣ�С�������Լ�ƿ��ǩ�ϱ�ע��������������Ϊ10%���ϱ��е��ܽ�������жϣ���ƿ�Լ���������____��Һ��
���������룩�ٿ�����NaCl��Һ���ڿ�����Na2CO3��Һ���ۿ�����_____��Һ��
����Ʒ�����ʵ�飩
(1)Сǿ�ýྻ�IJ�����պȡ����Һ����pH��ֽ�ϣ����pH��7������ƿ�Լ���������NaCl��Һ��
(2)СǿΪ�˽�һ����֤���룬���ֽ���������ʵ�飺
�������� | ʵ������ | ���� |
��ȡ��Ʒ���Թ��У��μ�_____ | ������������ | �������ȷ |
�ڰѲ���������ͨ�����ʯ��ˮ�� | �а�ɫ�������� |
����չ��Ӧ�ã�����ѡ����Сǿ��ͬ���Լ�����֤����ڳ�������ѡ��____��Һ��