题目内容
【题目】甲乙两位同学对化学实验非常感兴趣,请结合图表信息回答问题:

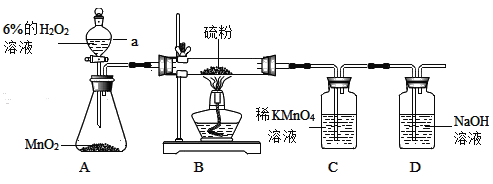
甲同学如图1研究二氧化碳的制备:
(1)仪器①的名称:_____________。
(2)实验室用石灰石与稀盐酸反应制取二氧化碳,他选用了A而没有选用F做发生装置,是因为A的优点是_________________。收集二氧化碳选用______(填字母),验满的方法是______________________。
(3)E装置的用途很广。下列关于该装置用法正确的是_____。
①当装置内盛满水,若收集氢气,气体从a通入;若收集氧气,气体从b通入。
②当装置内盛满氧气时,若将装置内的氧气排出来,水从b通入。
③当装置内盛有一半水时,可观察给病人输氧气的速率,b端连氧气钢瓶。
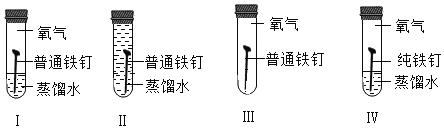
(4)用大理石和稀盐酸制得CO2中混有H2S,HCl等气体。获取纯净干燥CO2,如图2实验:[查阅资料] H2S能与NaOH、CuSO4等物质反应。
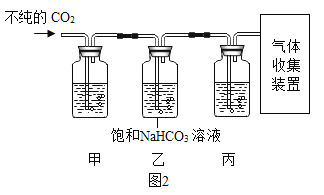
①装置甲中所盛试剂应选用________(填字母)。
a浓硫酸 bNaOH溶液 c澄清石灰水 dCuSO4溶液
②装置乙中发生反应的化学方程式_________ ,装置丙的作用是___________。
(5)乙同学研究了木条复燃与氧气体积分数的关系:乙同学发现不纯的氧气也能使带火星的木条复燃。他想收集一瓶混有约1/4体积空气的氧气,应该选用图3中___(填序号)完成实验,收集好后集气瓶中氧气的体积分数约为___(空气中氧气的含量按1/5计算)。
a.  集气瓶中灌1/4的水
集气瓶中灌1/4的水
b.  集气瓶中灌3/4的水
集气瓶中灌3/4的水
c.  导管伸入到集气瓶的1/4处
导管伸入到集气瓶的1/4处
d.  导管伸入到集气瓶的3/4处
导管伸入到集气瓶的3/4处
【答案】长颈漏斗 能够控制反应的发生与停止 C 用燃着的木条放在集气瓶口,如果木条熄灭,则说明收集满 ③ d NaHCO3+HCl=NaCl+H2O+CO2↑ 除去水蒸气 b 80%
【解析】
(1)仪器①的名称:长颈漏斗。
(2)实验室常用大理石(或石灰石)和稀盐酸反应制取二氧化碳,碳酸钙和稀盐酸反应生成氯化钙、水和二氧化碳,属于固、液常温型,他选用了A而没有选用F做发生装置,是因为A装置可以将固体放在多孔塑料片上,在试管中放入液体,两者接触可反应生成二氧化碳气体,若关闭导管上的止水夹,试管中的气体增多,压强增大,把液体压入长颈漏斗,固体和液体分离,反应停止;故A装置的优点是:能够控制反应的发生与停止;二氧化碳的密度比空气大,可用装置C向上排空气法收集;二氧化碳验满的方法是用燃着的木条放在集气瓶口,如果木条熄灭,则说明收集满。
(3)①当装置内盛满水,氢气、氧气密度都比水小,若收集氢气,气体从b通入;若收集氧气,气体从b通入,故选项错误;
②氧气密度比水小,当装置内盛满氧气时,将装置内的氧气排出来,水从b通入,故选项正确;
③当装置内盛有一半的水时,可观察给病人输氧气的速率,b端连氧气钢瓶,故选项正确。故选③。
(4)①H2S能与NaOH、CuSO4等物质反应;但氢氧化钠也能和二氧化碳反应,硫酸铜不和二氧化碳反应,所以装置甲中所盛试剂应选用CuSO4溶液;故选d。
②CO2中混有的HCl气体可用饱和NaHCO3溶液吸收,氯化氢和碳酸氢钠反应生成氯化钠、水、二氧化碳。装置乙中饱和NaHCO3溶液吸收HCl气体;发生反应的化学方程式NaHCO3+HCl=NaCl+H2O+CO2↑,装置丙中放置浓硫酸,用来干燥气体。
(5)想收集一瓶混有约![]() 体积空气的氧气,需要往集气瓶中装入
体积空气的氧气,需要往集气瓶中装入![]() 的水,应该选用图2中b完成实验,收集好后集气瓶中氧气的体积分数约为:
的水,应该选用图2中b完成实验,收集好后集气瓶中氧气的体积分数约为:![]() +
+![]() ×
×![]() ×100%=80%;不能用排空气法,因为排空气法气体混合使结果不准确。
×100%=80%;不能用排空气法,因为排空气法气体混合使结果不准确。

【题目】长期使用的热水锅炉会产生水垢。水垢主要成分是碳酸钙和氢氧化镁。某兴趣小组为了测定水垢中CaCO3的含量,将6g水垢粉碎放在烧杯中,然后向其中加入40g某浓度的稀盐酸,使之充分反应(水垢中除碳酸钙和氢氧化镁外都不与稀盐酸反应)。实验数据记录如下:
反应时间/min | 0 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
烧杯内所盛物 质的总质量/g | 46.0 | 45.2 | 44.8 | 45.1 | 44.1 | 43.9 | 43.8 | 43.8 | 43.8 |
试计算:(1)表中有一数据是不合理的,该数据的测得时间是第_____min;
(2)水垢中CaCO3的质量分数_____(计算结果精确至0.1%)。