题目内容
【题目】如图所示的四个图像,不能正确反映其对应变化关系的是( )
A. 用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气
用等质量、等浓度的过氧化氢溶液在有无催化剂条件下制氧气
B.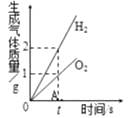 电解一定量的水
电解一定量的水
C. 一定质量的镁粉在密闭容器中燃烧
一定质量的镁粉在密闭容器中燃烧
D. 向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉
向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉
【答案】B
【解析】A.等质量、等浓度的过氧化氢溶液在有催化剂条件下比没有催化剂的条件下生成氧气的速度快,但二者生成的氧气的质量相等;A不符合题意;
B.电解水生成的氢气和氧气的体积比是2:1;B符合题意;
C.根据质量守恒定律,一定质量的镁粉在密闭容器中燃烧后物质的总质量不变;C不符合题意;
D.根据金属活动性顺序,向等质量、等浓度的稀硫酸中分别逐渐加入锌粉和铁粉,锌粉与稀硫酸反应的速度较快,生成的氢气的速度较快,最终稀硫酸完全反应,生成氢气的质量相等;D不符合题意.
故答案为:B.
A、用等质量、等浓度的双氧水分别制取氧气,有无催化剂只是改变化学反应的速率,不影响生成氧气的量;
B、水通电电解生成氢气和氧气的体积比为2:1;
C、红磷在密闭容器中燃烧质量不变;
D、相同质量的两种金属和等质量、等浓度的酸反应,金属越活泼,和酸反应的速率越快,金属的相对原子质量越小,产生的氢气越多.

 百年学典课时学练测系列答案
百年学典课时学练测系列答案【题目】某保健品的部分标签内容如图所示:
(1)根据所给信息可知该保健品主要功效中起主要作用的元素是(填元素符号)。
(2)食用方法中嚼食的目的是。
(3)某课外小组利用实验,探究该保健品中是否可能含有碳酸钙.请你帮助他们完成探究报告.实验室提供实验仪器如下: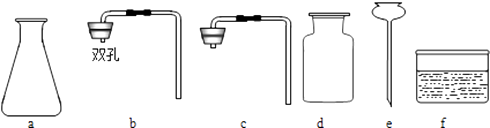
【猜想】该药品中含有碳酸钙.
【设计实验】
序号 | 实验主要步骤及部分现象 |
① | 选择药品:该保健品粉末、稀盐酸和; |
② | 连接仪器,(填实验步骤),装药品。 |
③ | 实验开始时,观察到有气泡产生,发生反应的化学方程式为 , 收集产生的气体。 |
④ | 验满:证明气体已收集满的方法是。 |
⑤ | 检验:检验收集到的这瓶气体的方法、现象及结论是 , 该反应的化学方程式为。 |
【结论】根据标签和实验,可初步推断,该药片中可能含有碳酸钙。
(4)【反思与拓展】实验结束后,小组同学将剩余药品进行了固、液分离,并检验了倒入废液缸中的废液,请你设计实验证明废液中不含稀盐酸(简述实验方法和现象)。。



