题目内容
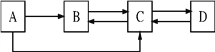
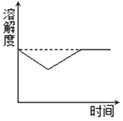
【题目】向盛有10g质量分数为49%稀硫酸的烧杯中加入5.6g的铁粉,充分反应后有固体残留,t1时迅速倒入一定量的硫酸铜溶液。整个过程烧杯中溶液的质量随时间的变化如图所示。分析错误的是( )
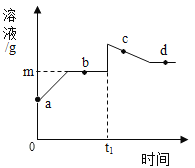
A.a→b点,溶液的pH逐渐增大
B.取b点时的溶液,加入锌粉,无气泡放出
C.c点时,溶液中有两种溶质
D.d点固体,加入盐酸有气泡产生
【答案】D
【解析】
由方程式:
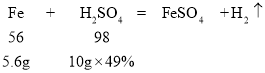
可知,向盛有10g49%稀硫酸的烧杯中加入5.6g克的铁粉,铁粉有剩余,在t1时迅速倒入一定量的硫酸铜溶液,铁与硫酸铜反应溶液的质量减小。
A、由上述分析和图象可知,a→b点,溶液的酸性减弱,其pH逐渐增大,选项分析正确;故不符合题意;
B、由上述分析和图象可知,b点时溶液中没有剩余的稀硫酸,加入锌粉,没有气体放出,选项分析正确;故不符合题意;
C、由图象可知,c点时溶液的质量还在减小,硫酸铜没有完全反应,溶液中溶质有硫酸亚铁和硫酸铜两种,选项分析正确;故不符合题意;
D、由于硫酸铜的量不能确定,可能有剩余的铁,d点时,烧杯中固体一定是有铜,可能有铁,加入盐酸不一定有气泡产生,选项分析错误;故符合题意;
故选D

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】硝酸钾的部分溶解度数据见下表。
温度(℃) | 10 | 20 | 40 | 60 |
溶解度(g/100g 水) | 20.9 | 31.6 | 63.9 | 110 |
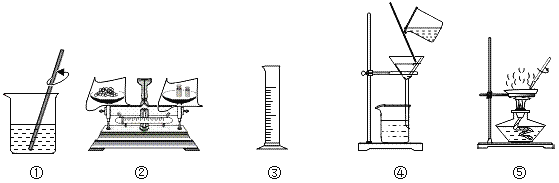
①20℃时,称取 10.0 克硝酸钾固体加入到 40 克水中,用_____(写出仪器名称)搅拌,充分溶解后得到_____(选填“饱和”或“不饱和”)溶液。
②将上述溶液升温至 60℃,所得溶液的溶质质量分数为_____。
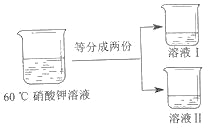
③将 60℃的硝酸钾溶液进行如图所示操作。
将溶液 I 降温,开始析出硝酸钾晶体的温度介于_____℃(选填编号之间。
A. 40-60 B. 20-40 C. 10-20 D. 低于 10
为得到 60℃时硝酸钾饱和溶液,将溶液 II 恒温蒸发 15 克水,请分析该操作能否达到实验目的并说明理由_____。