��Ŀ����
����Ŀ��ijʵ��С���ͬѧҪ��BaCl2��NaCl�����Һ�еõ��ϴ�����BaCl2��NaCl���壬Ϊ�˽�������ʵ����ƺͲ�������ش��������⡣
��������⣩��η���BaCl2��NaCl�����õ����־��壿
����Ʒ�����ʵ�飩
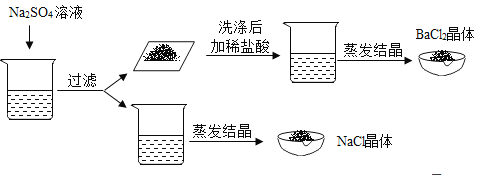
����ͬѧ��ʵ�鷽����ȡһ���ֻ��Һ���Թ��У��������м���������Na2SO4��Һ�����ˣ��������м�������ϡ���ᣬ����Һ�����ᾧ��
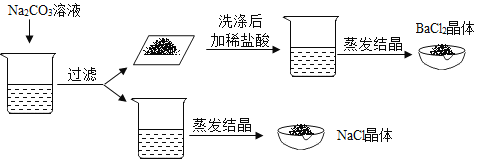
С��ͬѧ��ʵ�鷽����ȡһ���ֻ��Һ���Թ��У��������м��������Na2CO3��Һ�����ˣ��������м������ϡ���ᣬ����Һ�����ᾧ��
����дʵ�鱨�棩
(1)��д������ͬѧ����Na2SO4��Һ��Ӧ�Ļ�ѧ����ʽ___
(2)С��ͬѧ���������ټ������ϡ�����ʵ��������___��
�����������ۣ�
(3)С��ͬѧ��Ϊ����ͬѧʵ�鷽����������������___
(4)С��ͬѧ��ʵ���м��������Na2CO3��Һ��������Һ�е�������___(�����ӷ���) ����ͬѧ��Ϊ�������ϡ�������̼��������ȥ������������ʹ���õ��Ȼ�����Һ�����������ӣ����Է�������������С��ͬѧ��ΪֻҪ����Һ���������ᾧ�Ͳ���Ӱ��ʵ�������ڽ�����������ʱ����___��ֹͣ���ȡ�
����˼���ܽᣩ
(5)С��ͬѧ�ڽ��в���ʱ�����Լ����ǹ����ģ��������õ�����ȷ�Ǵ����ģ��ɴ����ǵó��ľ����ǣ��������ǰ������Լ����ܿ�����������ô����ͨ��___��ȥ�������ӣ����������������ӻ�����������ӡ�
���𰸡�BaCl2+Na2SO4�TBaSO4��+2NaCl ��ɫ�������ܽ⣬�������� �����м���������Na2SO4��Һʱ�������ƺ��Ȼ�����Ӧ���ɰ�ɫ�������ᱵ�����ˣ��������м�������ϡ����ʱ�����ᱵ���ܺ�ϡ���ᷴӦ����˲��ܵõ��Ȼ������� Na+��Cl����CO32�� ���ֽ϶����ʱ ���������Լ���ǰ�����Ĺ����Լ���Ӧ
��������
(1)�Ȼ����������Ʒ�Ӧ�������ᱵ�������Ȼ��ƣ���˷�Ӧ�ķ���ʽΪ��BaCl2+Na2SO4�TBaSO4��+2NaCl��
(2)̼�ᱵ�����ᷴӦ�����Ȼ�����ˮ�Ͷ�����̼����˻�۲쵽������Ϊ����ɫ�������ܽ⣬�������ݣ�
(3)���������ƺ��Ȼ�����Ӧ���ɰ�ɫ�������ᱵ�������ᱵ�������ᷴӦ����˲��ܵõ��Ȼ��������ԣ������м���������Na2SO4��Һʱ�������ƺ��Ȼ�����Ӧ���ɰ�ɫ�������ᱵ�����ˣ��������м�������ϡ����ʱ�����ᱵ���ܺ�ϡ���ᷴӦ����˲��ܵõ��Ȼ������壻
(4)̼���ƺ��Ȼ�����Ӧ����̼�ᱵ�������Ȼ��ƣ������Һ�к����Ȼ����е������Ӻ������ӣ��ҹ�����̼���ƣ����к��е�����Ϊ�����Ӻ�̼������ӣ������Һ�к��������ӡ������Ӻ�̼������ӣ�����Ϊ��Na+��Cl����CO32��������ʱҪ�ȵ����ִ�������ʱֹͣ���ȣ������Ⱥ�ɣ�
(5)�ڽ��в���ʱ�����Լ��������ǹ����ģ�Ҫ�õ������Ǵ����ģ�����ͨ�����������Լ���ǰ�����Ĺ����Լ���Ӧ��ȥ�������ӣ����������������ӻ�����������ӡ�

 �ִʾ�ƪ��ͬ�����Ĵ��ϵ�д�
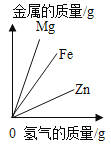
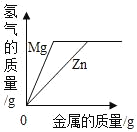
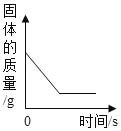
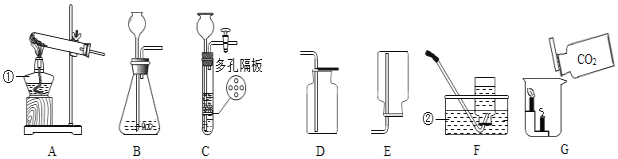
�ִʾ�ƪ��ͬ�����Ĵ��ϵ�д�����Ŀ������ͼ������ȷ��ӳ��Ӧ�仯��ϵ���ǣ�������
|
|
|
|
Mg��Zn��Fe��ϡ���ᷴӦ | ������������������������������þ�ۡ�п�� | ��ͭƬ����һ��������������Һ�� | ��һ���������Ȼ�п��������Һ�м���п�� |
A. A B. B C. C D. D
����Ŀ������ѧУ��Ԫ���������ϣ�ijͬѧ��������ˮ����������ħ����������й�������(Na2O2)��ĩ����֬���ϵ�ˮ����֬��ȼ����������Сӱ������λ���dz�����Ȥ������ͬѧ��һ��Ը����������һϵ�е�̽����
[�������]����������ˮ��Ӧ������ʲô���ʣ�Ϊʲô��֬��ȼ�գ�
[�� ��]��������һ���������һ��������������Ӧ�����п����������仯
[���װ��]��ͼ��ʾ

[ʵ��̽��]
ʵ��һ��̽����Ӧ�����ɵ�������ʲô��
(1)����ͼװ���з�Һ©���Ļ��������Ƶμ�ˮ���ٶȣ��۲쵽�Թ��������ݲ������ô����ǵ�ľ������P����ľ����ȼ��˵�����ɵ�������________��
(2)ʵ���У����۲쵽�����ձ��еĵ��ܿ�������ð��������Ͳ����������ԭ��______________��
ʵ�����̽����Ӧ�����ɵ���һ��������ʲô��
(1)С��������һ��������Na2CO3��С����Ϊ�����ܡ�Ϊ��֤ʵС���Ŀ������������һ��֤��Na2CO3�����ڵ�ʵ�飺
ʵ�鲽�� | ʵ������ | ʵ����� |
_________ | _________ | ��������û�� |
(2)С��ȡ��Ӧ�����õ���Һ���Թ��У�������ɫ��̪��Һ�������Թ��е���Һ��ɺ�ɫ��˵����Ӧ�����õ���Һ��________�ԡ�
[����]С������ʵ��̽���Ľ����д���˹������ƺ�ˮ��Ӧ�Ļ�ѧ����ʽΪ_________________��