题目内容
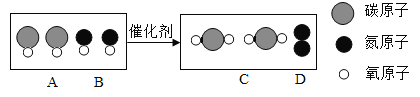
【题目】如图是某反应的微观示意图,该反应的化学方程式为________________________;反应前后化合价升高的元素为_________________________。
【答案】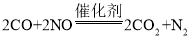 C
C
【解析】
由图可知,反应物含2个一氧化碳分子,2个一氧化氮分子,生成物中含2个二氧化碳分子,1个氮分子,故该反应的化学方程式为: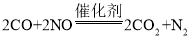 ;
;
反应前,CO中氧元素的化合价为-2价,设碳的化合价为x,根据化合物中正、负化合价的代数和为零,可得x+(-2)=0,x=+2;NO中氧元素的化合价为-2价,设氮元素的化合价为y,根据化合物中,正、负化合价的代数和为零,可得y+(-2)=0,y++2;
生成物中,氮元素的化合价为0;二氧化碳中氧元素的化合价为-2价,设二氧化碳中碳元素的化合价为z,根据化合物中,正、负化合价的代数和为零,可得z+(-2)×2=0,z=+4,故化合价升高的元素为:C。

练习册系列答案
 开心试卷期末冲刺100分系列答案
开心试卷期末冲刺100分系列答案 双基同步导航训练系列答案
双基同步导航训练系列答案 黄冈小状元同步计算天天练系列答案
黄冈小状元同步计算天天练系列答案
相关题目
【题目】实验室有一瓶标签模糊的氢氧化钠溶液,为了测定其溶质质量分数,小明进行了如下实验:①取一洁净的锥形瓶称量,然后往其中加入一定量的氢氧化钠溶液,并滴入几滴酚酞试液(质量忽略不计),重新称量;②往上述锥形瓶中加入溶质质量分数为7.3%的盐酸,边加边振荡,溶液红色褪去时,再次称量。数据如下表:回答下列问题:
锥形瓶/g | 锥形瓶+氢氧化钠溶液/g | 锥形瓶+反应后溶液/g | |
质量/g | 35.5 | 60.5 | 110.5 |
(1)根据表中数据,通过计算确定该瓶氢氧化钠溶液的溶质质量分数_________。
(2)小建用pH试纸测得小明实验反应后锥形瓶内溶液的pH为4,则小明测出氢氧化钠溶液的质量分数比实际浓度_________(选填“偏大”或“偏小”),造成这一偏差的原因是________。