题目内容
【题目】如图所示为实验室中常见的气体制备和收集装置,请回答下列问题:
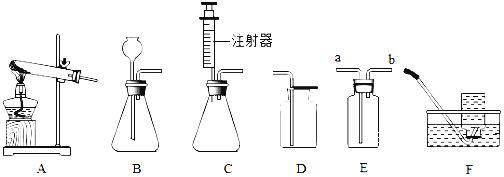
(1)用加热氯酸钾与二氧化锰混合物制氧气,可选用的发生装置是_____(填字母序号);若要收集较为纯净的氧气,应选择的装置是________(填字母代号)
(2)实验室制氧气还可以用高锰酸钾,它是一种紫黑色的晶体,其制取氧气的符号表达式为________________________________________,该反应属于_____反应(基本反应类型).如用其制氧气并用排水法收集,停止加热时要先把_____,其目的是__________;如发现水槽中的水变成了浅紫红色,你认为产生该现象的原因可能是_____.
(3)欲使用装置E用排空气法收集氧气,则气体应从_____(填“a”或“b”,下同)端通入,验满的方法是___________________;欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从_____端通入.
(4)用B作为反应发生装置制取氧气时反应的符号表达式是___________________.若选用C做发生装置,你认为 选用C的优点是_____.
(5)1班同学对探究影响反应快慢的一些因素的收集了相关数据(常温通常指20℃;)
实验序号 | 过氧化氢溶液浓度/% | 过氧化氢溶液质量/g | 温度/℃ | 二氧化锰用量/g | 氧气体积/ml | 反应所需时间/s |
a | 5 | 12 | 20 | 0.2 | 125 | 11 |
b | 30 | 12 | 20 | 0.2 | 125 | 2 |
c | 30 | 12 | 40 | / | 125 | 148 |
d | 30 | 12 | 90 | / | 125 | 82 |
通过实验a和b对比可知,化学反应快慢与 __ 有关;通过对比实验可知,化学反应快慢与温度的关系是________________。
(6)对于过氧化氢分解制取氧气,硫酸铜溶液和硫酸铁溶液也有一定的催化作用,为比较硫酸铁和硫酸铜对过氧化氢分解的催化效果,甲乙两组的同学分别设计了如图甲、乙所示的实验.请回答相关问题:
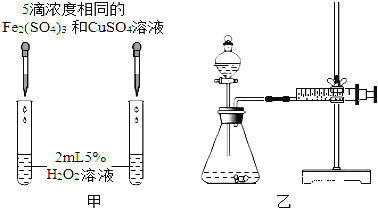
①如图甲,可通过观察 __ 定性比较两者的催化效果.
②如图乙(装置气密性良好),要定量比较两者的催化效果,可测量________
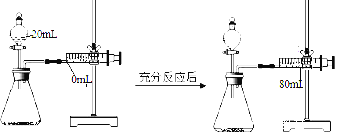
③用乙装置还可知生成的氧气的质量(装置气密性良好).下列分析错误的是 __
A、通过测定氧气的体积计算氧气的质量
B、注射器中收集到的气体是氧气
C、反应后,共生成了80mL O2
D、反应后需要等装置冷却到室温再读数.
【答案】 A F 2KMnO4![]() K2MnO4+MnO2+O2↑ 分解反应 先把导管移出水面再熄灭酒精灯 防止水倒流使试管炸裂 试管口没有赛棉花 a 将带火星的木条放在导管b 处,若带火星的木条复燃则已满 【答题空10】b 2H2O2
K2MnO4+MnO2+O2↑ 分解反应 先把导管移出水面再熄灭酒精灯 防止水倒流使试管炸裂 试管口没有赛棉花 a 将带火星的木条放在导管b 处,若带火星的木条复燃则已满 【答题空10】b 2H2O2![]() 2H2O+O2↑ 控制化学反应速率 反应物的浓度 温度越高反应速率越快 产生气泡的快慢 产生相同体积的气体所需的反应时间 BC
2H2O+O2↑ 控制化学反应速率 反应物的浓度 温度越高反应速率越快 产生气泡的快慢 产生相同体积的气体所需的反应时间 BC
【解析】(1)用加热氯酸钾与二氧化锰混合物制氧气,可选用的发生装置是固固加热型A;若要收集较为纯净的氧气,应用排水集气法收集,选择的装置是F;(2)高锰酸钾在加热条件下分解生成氧气、二氧化锰、锰酸钾,符号表达式为2KMnO4△ K2MnO4+MnO2+O2↑,该反应属于分解反应。如用其制氧气并用排水法收集,停止加热时要先把导管移出水面,再熄灭酒精灯,其目的是防止水倒流使试管炸裂;如发现水槽中的水变成了浅紫红色,产生该现象的原因可能是试管口没有赛棉花,使高锰酸钾颗粒进入水槽。(3)欲使用装置E用排空气法收集氧气,由于氧气的密度比空气大,则气体应从 a端通入,验满的方法是将带火星的木条放在导管b 处,若带火星的木条复燃则已满;欲使用装置E用排水法收集氧气,先将瓶中装满水,再将气体从b端通入;(4)过氧化氢法制氧气用B作为反应发生装置,反应的符号表达式是2H2O2 MnO2 2H2O+O2↑.若选用C做发生装置,你认为 选用C的优点是控制液体的滴加速率,进而控制反应速率;(5) 通过实验a和b对比可知,化学反应快慢与过氧化氢溶液的浓度有关,浓度越大,反应越快;化学反应快慢与温度的关系是温度越高,反应速率越快;(6) ①如图甲,可通过观察 产生气泡的快慢定性比较两者的催化效果;②如图乙(装置气密性良好),要定量比较两者的催化效果,可测量产生相同体积的气体所需的反应时间;③A、通过测定氧气的体积计算氧气的质量,正确;B、刚开始从发生装置排出的是装置内的空气,注射器中收集到的气体是氧气和空气的混合物,或者都是空气;C、反应后,生成的氧气体积小于80mL ,注射器内收集气体的体积等于生成的氧气和进入装置的液体的体积和;D、反应后需要等装置冷却到室温再读数,否则因气体的热胀冷缩导致结果不准确。

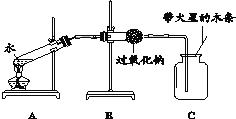
【题目】在元旦联欢晚会上,化学老师表演了“吹气生火”的魔术。用棉花将淡黄色的过氧化钠(Na2O2)固体包在其中,将一根长玻璃管插入棉花团中吹气,棉花团剧烈燃烧起来。为了揭开魔术的秘密,同学们进行了如下探究。
【提出问题】过氧化钠与人呼出的哪种气体发生反应?
【查阅资料】
① 人呼出的气体中主要成分是N2、O2、CO2和水蒸气等。
② NaOH溶液能与CO2反应但与O2不反应。
【作出猜想】
① 过氧化钠与人呼出的N2反应并生成O2。
② 过氧化钠与人呼出的水蒸气反应并生成O2。
③ 过氧化钠与人呼出的CO2反应并生成O2。
【进行实验】
序号 | 实验装置 | 实验现象 |
实 验 1 |
|
|
实 验 2 |
| 带火星的木条复燃 |
实 验 3 |
| 带火星的木条复燃 |
【解释与结论】
(1)实验1中,观察到____________________,可判断猜想①不成立。
(2)实验2中,A装置中发生的变化是__________(填“物理变化”或“化学变化”)。
(3)实验3中,B装置所盛试剂及其作用是_____________________。
(4)由上述3个实验可判断,猜想②、③成立。已知实验2中另一种产物由3种元素组成,写出该反应的符号表达式_______________________。
【反思与评价】
与学过的实验室制氧气相比,过氧化钠更适合在潜水艇中使用,其优点是_______________。
[计算题](需要用到的相对原子质量请到卷首查)