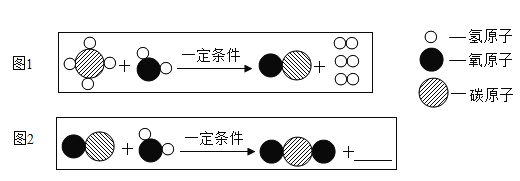
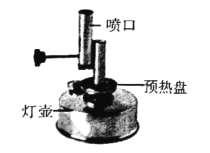
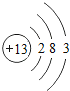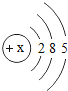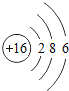题目内容
【题目】认识和爱护水资源
(1)水的净化
天然水中含有许多杂质,可利用吸附沉淀、_____和蒸馏等方法净化。
(2)水的软化
硬水给生产和生活带来很多麻烦,生活中常用_________________降低水的硬度。
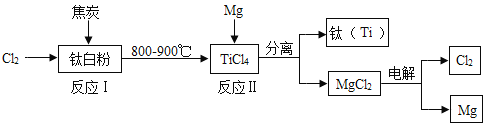
(3)水的蒸馏
实验室制取蒸馏水的装置如图所示。
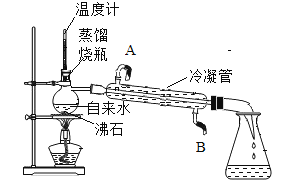
①在蒸馏烧瓶中加入几粒沸石(或碎瓷片)的作用是____________。
②冷水应从冷凝管的_______________(填A或B)端进入。
③从微观角度分析,冷凝管中的水蒸气与锥形瓶中的水不同之处为_____________(写一条)。
(4)水的饮用
某品牌矿泉水,其外包装上部分文字说明如图所示。
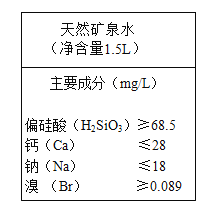
①主要成分中的“钙”“钠”是指_______________(“分子” “原子”或“元素”)。
②偏硅酸中硅元素的质量分数是_________________(列式即可)。
③每瓶矿泉水中含钙的质量最多为______________mg。
【答案】过滤 煮沸 防止暴沸(局部沸腾) B 分子间间隔不同(或分子运动速率不同) 元素 ![]() 42
42
【解析】
(1)天然水中含有许多杂质,可利用吸附沉淀、过滤和蒸馏等方法净化;
(2)天然水煮沸时,水中可溶性钙、镁化合物转化为沉淀,水的硬度降低。生活中常用煮沸降低水的硬度;
(3)①在蒸馏烧瓶中加入几粒沸石(或碎瓷片)的作用是防止暴沸(局部沸腾);
②为提高冷却效率,冷水应从冷凝管的B端进入;
③从微观角度分析,冷凝管中的水蒸气与锥形瓶中的水不同之处为分子间间隔不同(或分子运动速率不同);
(4)①主要成分中的“钙”“钠”是指元素;
②偏硅酸中硅元素的质量分数=![]() ;
;
③根据标签可知,每瓶矿泉水中含钙的质量最多=28 mg/L×1.5L=42mg。

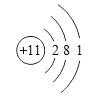
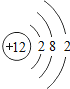
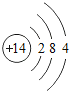
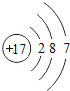
【题目】下表为元素周期表中某一周期元素的原子结构示意图。
元素名称 | 钠 | 镁 | 铝 | 硅 | 磷 | 硫 | 氯 | 氩 |
元素符号 | Na | Mg | Al | Si | P | S | CI | Ar |
原子结构示意图 |
|
|
|
|
|
|
|
|
请回答下列问题:
(1)表中磷原子的核电荷数x=____________;
(2)表中具有相对稳定结构的元素是______________;
(3)在化学反应中,每个铝原子失去________________个电子形成铝离子;
(4)镁元素与氟元素形成化合物的化学式为___________________;
(5)上述元素在周期表中处于第________________周期,处于同一周期的原因是_______________。