题目内容
【题目】二氧化碳是重要的资源。
(1)植物生长离不开二氧化碳,有人说光合作用是地球上最伟大的化学变化,写出化学方程式_____。
(2)某同学对二氧化碳的某种性质作了如下探究:

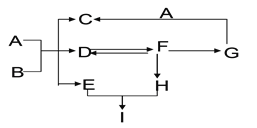
如图所示,在C处放入用石蕊溶液染成紫色的干燥的纸花完成以下实验:在A处持续而缓缓地通入气体X。当关闭K时,C处的紫色石蕊纸花不变色;当打开K后,C处的紫色石蕊纸花变为红色。若气体X为未经干燥的二氧化碳,则B瓶中盛放的溶液可以为_____(填字母)。
A 浓硫酸
B 氢氧化钠溶液
C 饱和碳酸氢钠溶液
【答案】6CO2+6H2O C6H12O6+6O2 AB
C6H12O6+6O2 AB
【解析】
(1)二氧化碳与水在有光照和叶绿素的条件下产生葡萄糖和氧气的化学方程式6CO2+6H2O C6H12O6+6O2。
C6H12O6+6O2。
(2)
A、浓硫酸,具有吸水性,能干燥二氧化碳气体,干燥的二氧化碳不能使C中石蕊纸花变红;故选项正确;
B、氢氧化钠溶液能与二氧化碳反应产生碳酸钠和水,不能是二氧化碳气体进入C装置,则C装置中的石蕊纸花不变红;故选项正确
C、饱和碳酸氢钠溶液,不能与二氧化碳反应,且二氧化碳气体从溶液中排出一定含有水蒸气,可以使C装置中的石蕊纸花变红;故选项错误;
故选:AB。

 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案 开心蛙口算题卡系列答案
开心蛙口算题卡系列答案【题目】某校化学研究性学习小组探究气体制取的实验原理与方法.
(1)甲同学将课本的基础知识进行整理如图,请你帮助他完成相关内容.

制取气体 | 所需要品 | 装置连接顺序 | 反应的化学方程式 |
二氧化碳(干燥) | 大理石和稀盐酸 | ______________ | ______________________________ |
(2)乙同学设计的实验装置(如图),既可用于制取气体,又可用于验证物质性质.当打开K1、关闭K2时,利用I、Ⅱ装置可直接进行的实验是______________(填序号).
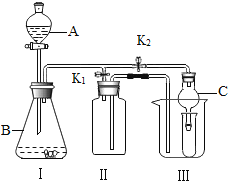
①大理石与稀盐酸反应制取二氧化碳
②锌与稀硫酸反应制取氢气
(3)丙同学认为在不改变I、Ⅱ、Ⅲ装置的仪器及
位置的前提下,该装置可用于过氧化钠(Na2O2)与水反应制取氧气,另一产物为氢氧化钠,则该反应的化学方程式为:______________________________;她的改进措施是_______________________________________________________.
(4)丁同学打开K2、关闭K1,利用I、Ⅲ装置来验证生成的二氧化碳中含有水蒸气,此时C中盛放的物质是_______________,可以观察到的现象是________________________________________.
(5)对用氯酸钾和二氧化锰的混合物制取O2后的固体残渣(假定已完全反应)作如下回收处理:
①通过以下四步实验操作回收二氧化锰.正确操作的先后顺序是____________(填写选项序号).
a.烘干b.溶解c.过滤d.洗涤
②用所得氯化钾晶体配制50g质量分数为5%的氯化钾溶液,需要氯化钾的质量为_______g.
③过滤、蒸发时都需用到的仪器是__________(填序号).
A.酒精灯B.烧杯C.玻璃棒D.漏斗E.量筒
(6)小明用6.5g可能含有铜、铝、铁、镁中的一种或几种金属杂质的锌粉,跟足量的稀盐酸完全反应时,生成0.2g氢气,则此锌粉中一定含有的金属杂质是________________.