题目内容
某课外活动小组的同学将过量的炭粉和16克氧化铜均匀混合,用下图所示装置
进行实验.图中铁架台等装置已略去.请回答有关问题:
(1)同学们想通过测定消耗碳、氧元素的质量和生成二氧化碳的质量,分析氧化铜和炭粉反应产生的气体除CO2外是否还有其它产物.反应一段时间后停止加热,冷却到室温.反应前、后测得的数据如下:
| 装置 | 反应前 | 反应后 |
| A | 试管的质量38.2 克 氧化铜和炭粉混合物的质量20.0克 | 试管和固体物质的质量56.8 克 |
| B | 反应后瓶内石灰水比反应前增重1.1 克 | |
A.装置中还有一部分CO2未被石灰水溶液吸收
B.氧化铜和炭粉反应产生的气体除CO2外还有CO
C.氧化铜和炭粉没有完全反应
D.该反应不符合质量守恒定律
(2)有同学认为用图示装置C代替上面的装置A,加热前先通一会气体X,停止加热后再通一会该气体,这样可使实验测得的数据更能准确的说明问题.你认为在O2、N2和H2三种气体中,X应选择哪一种气体?______.
(3)实验中最多能得到铜多少克?(写出计算过程)
【答案】分析:(1)根据质量守恒定律求出反应前后的质量差和1.1g比较进行分析.
可从反应条件及装置中气体是否被充分吸收角度进行分析.
(2)根据X是否参与反应影响实验及安全性角度分析.
(3)根据化学方程式进行计算,注意解题步骤的规范性.
解答:解:(1)根据质量守恒定律知反应前后的质量差即为反应的碳和氧的质量,为56.8g-38.2g-20.0g=1.4g>1.1g,说明反应中消耗碳和氧元素的质量大于生成二氧化碳的质量.主要原因是由于装置的滞留的二氧化碳不能被吸收,同时反应时还可能发生反应C+CuO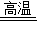 Cu+CO↑,部分碳没有转换为二氧化碳.
Cu+CO↑,部分碳没有转换为二氧化碳.
故答案为:大于; AB
(2)因为氧气要和碳发生反应,反应结束后要和生成的铜反应,影响实验结果;
氢气具有可燃性,且不安全使用时必须验纯,所以选氮气.
故答案为:N2
(3)解:设实验中最多能得到铜的质量为X
C+2CuO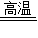 2Cu+CO2↑
2Cu+CO2↑
160 128
16g X

解之得:X=12.8g
答:实验中最多能得到铜的质量为12.8g
点评:根据化学方程式进行计算,关键要注意步骤规范,一般步骤为:①设未知量,②正确书写化学方程式,③找出已知量,未知量,算有关的相对分子质量,④列比例式,⑤解比例式,⑥简答.
可从反应条件及装置中气体是否被充分吸收角度进行分析.
(2)根据X是否参与反应影响实验及安全性角度分析.
(3)根据化学方程式进行计算,注意解题步骤的规范性.
解答:解:(1)根据质量守恒定律知反应前后的质量差即为反应的碳和氧的质量,为56.8g-38.2g-20.0g=1.4g>1.1g,说明反应中消耗碳和氧元素的质量大于生成二氧化碳的质量.主要原因是由于装置的滞留的二氧化碳不能被吸收,同时反应时还可能发生反应C+CuO
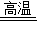 Cu+CO↑,部分碳没有转换为二氧化碳.
Cu+CO↑,部分碳没有转换为二氧化碳.故答案为:大于; AB
(2)因为氧气要和碳发生反应,反应结束后要和生成的铜反应,影响实验结果;
氢气具有可燃性,且不安全使用时必须验纯,所以选氮气.
故答案为:N2
(3)解:设实验中最多能得到铜的质量为X
C+2CuO
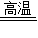 2Cu+CO2↑
2Cu+CO2↑ 160 128
16g X

解之得:X=12.8g
答:实验中最多能得到铜的质量为12.8g
点评:根据化学方程式进行计算,关键要注意步骤规范,一般步骤为:①设未知量,②正确书写化学方程式,③找出已知量,未知量,算有关的相对分子质量,④列比例式,⑤解比例式,⑥简答.

练习册系列答案
 口算与应用题卡系列答案
口算与应用题卡系列答案 名师点睛字词句段篇系列答案
名师点睛字词句段篇系列答案
相关题目
某课外活动小组的同学将过量的炭粉和16克氧化铜均匀混合,用下图所示装置进行实验.图中铁架台等装置已略去.请回答有关问题:
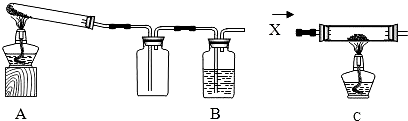
(1)同学们想通过测定消耗碳、氧元素的质量和生成二氧化碳的质量,分析氧化铜和炭粉反应产生的气体除CO2外是否还有其它产物.反应一段时间后停止加热,冷却到室温.反应前、后测得的数据如下:
分析数据发现,反应中消耗碳和氧元素的质量 (填“大于”、“小于”或“等于”)生成二氧化碳的质量.下列4项中跟这一结果有关的有哪几项? .(填写字母)
A.装置中还有一部分CO2未被石灰水溶液吸收
B.氧化铜和炭粉反应产生的气体除CO2外还有CO
C.氧化铜和炭粉没有完全反应
D.该反应不符合质量守恒定律
(2)有同学认为用图示装置C代替上面的装置A,加热前先通一会气体X,停止加热后再通一会该气体,这样可使实验测得的数据更能准确的说明问题.你认为在O2、N2和H2三种气体中,X应选择哪一种气体? .
(3)实验中最多能得到铜多少克?(写出计算过程)

(1)同学们想通过测定消耗碳、氧元素的质量和生成二氧化碳的质量,分析氧化铜和炭粉反应产生的气体除CO2外是否还有其它产物.反应一段时间后停止加热,冷却到室温.反应前、后测得的数据如下:
| 装置 | 反应前 | 反应后 |
| A | 试管的质量38.2 克 氧化铜和炭粉混合物的质量20.0克 |
试管和固体物质的质量56.8 克 |
| B | 反应后瓶内石灰水比反应前增重1.1 克 | |
A.装置中还有一部分CO2未被石灰水溶液吸收
B.氧化铜和炭粉反应产生的气体除CO2外还有CO
C.氧化铜和炭粉没有完全反应
D.该反应不符合质量守恒定律
(2)有同学认为用图示装置C代替上面的装置A,加热前先通一会气体X,停止加热后再通一会该气体,这样可使实验测得的数据更能准确的说明问题.你认为在O2、N2和H2三种气体中,X应选择哪一种气体?
(3)实验中最多能得到铜多少克?(写出计算过程)

 (2012?海珠区一模)某课外活动小组的同学为测定一瓶BaCl2溶液溶质的质量分数,做了以下实验,请回答有关问题:
(2012?海珠区一模)某课外活动小组的同学为测定一瓶BaCl2溶液溶质的质量分数,做了以下实验,请回答有关问题: