��Ŀ����
����Ŀ��(10��)��֪ij������Ʒ�к�����ɳ��Na2SO4��MgCl2��CaCl2�����ʡ�ʵ�����ᴿ�Ȼ��Ƶ��������£�
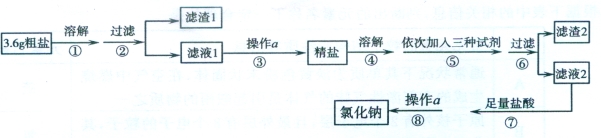
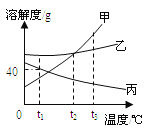
��1���ڢٲ�����ʱ����ˮ�����ʹ����ԼΪ (��֪20��ʱNaCl���ܽ��Ϊ36g)��
��������ˮ��������Ȼ�ܼӿ���ε��ܽ⣬��������IJ�������� ��ʵ��ʱ��������Ȼ���û�дﵽ���ͣ��þ��β��� (��䡢ƫ��ƫС)
��2���ڢڲ�����ʱ�������õ��������������÷ֱ��� �� ��
��3���ڢݲ����������Լ���˳����
A���������������ơ��������Ȼ�����������̼����
B���������Ȼ������������������ơ�������̼����
C��������̼���ơ��������Ȼ�������������������
D���������Ȼ�����������̼���ơ���������������
��4���ڢۢಽ����a�������� ���˲������У������ʹ�ò�������������ʹ���� (��䡢ƫ��ƫС)��
��5���ڵڢ߲������У�����Һ�еμ����������Ŀ����(�û�ѧ��Ӧ����ʽ��ʾ)
���𰸡���1��lOmL �����ں��������ܼ��������ܼ�ʱ������ӳ�������ȼ�� ����
��2��ѹƽ��ֽ ����
��3��A B D
��4������ ƫС
��5��Na2CO3+2HCl===2NaCl+H2O+CO2�� NaOH+HCl===NaCl+H20
��������
�����������1��20��ʱNaCl���ܽ��Ϊ36g ������100gˮ������ܽ�36gNaCl������Ҫ��ȫ3.6g��������ˮ�����ʹ����ԼΪlOmL����������ˮ��������Ȼ�ܼӿ���ε��ܽ⣬��������IJ�������ǣ������ں��������ܼ��������ܼ�ʱ������ӳ�������ȼ�ϣ�ʵ��ʱ��������Ȼ���û�дﵽ���ͣ�����Ӱ�����õľ����������ʵþ��β��ʣ�����
��2���ڢڲ����˲�����Ϊ��ʹ��ֽ�ܹ�����©���ڱڣ�ʹ�������ʸ��죬�ʵ�һ���õ��������������ǣ�ѹƽ��ֽ��ʹ��ֽ�ܹ�����©���ڱڶ����������ݣ��ڶ����õ������������ã�����
��3���ڢݲ����������Լ���Ŀ���ǵ�˳���dz�ȥNa2SO4��MgCl2��CaCl2���ʣ�Na2SO4���������Ȼ�������ȥ��MgCl2���������������Ƴ�ȥ��CaCl2��������̼���Ƴ�ȥ������������̼���ƻ�Ҫ��ȥ�������Ȼ���������̼����һ��Ҫ���Ȼ���֮����룬�ʿ�ѡA��B��D
��4���ڢۢಽ�������Ǵ���Һ�нᾧ�������壬�������������˲������У������ʹ�ò�������������Һ�ֲ����ȶ��ɽ���������ʹ����ƫС
��5���ڵڢ߲������У�����Һ�еμ����������Ŀ���ǣ��ǽ��������������ơ�̼���Ƴ�ȥ����ѧ����ʽΪ��Na2CO3+2HCl===2NaCl+H2O+CO2����NaOH+HCl===NaCl+H20

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�����Ŀ��������֤���ڻ�ѧ�仯�з��ӿ��ٷֵ���
A��ˮ���ȱ��ˮ���� B�����ưѵ�������
C������ѹ����Ƭ D��ˮͨ����������������
����Ŀ����9�֣�ij�о�С����������ᾧ����Ʒ�ֽ������ⶨ��Ʒ�в��ᾧ��������������������ʲ����뷴Ӧ�������ᾧ�壨H2C2O4��2H2O���IJ����������ʼ��±���
�� �� | �� �� | �� �� �� �� | �� �� �� Ӧ |
101����102�� | 150����160�� ���� | 100.1���ֽ��ˮ��175���ֽ��CO2��CO��H2O | �� Ca(OH)2��Ӧ������ɫ����(CaC2O4) |
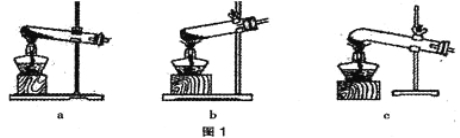
��1��ͼ1�Ǽ���װ�á������˵ļ��ȷֽ���ᾧ��װ���� ��
��2��ͼ 2 ����֤�ȷֽ�����к� CO ��CO2��װ�á�
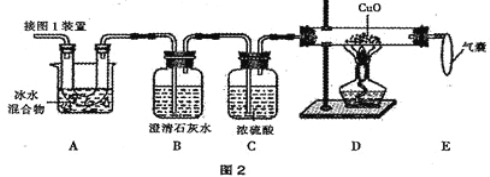
��װ�� A ����Ҫ������_______________ _ _____��
�����ҵ�������____________________��
��֤������ CO2��������_ ��B�з�Ӧ�Ļ�ѧ����ʽ ��
��֤������ CO ��������_______ _______��
��3��Ϊ�ⶨ��Ʒ�в��ᾧ�������������������·�������ȡһ������Ʒ��������װ�ý���ʵ�飬����װ��D��Ӧǰ�����������˼������ʵ������ʵ��ֵƫ�ͣ��ų������Ͳ������أ������ԭ��_______��дһ�����ɣ���
��4����ȡ17.5g���ᾧ����Ʒ����50.00g��Һ����������ϡ���ᣬȻ��μ�KMnO4 ��Һ����KMnO47.9�ˣ� ǡ�÷�Ӧ��ȫ��
����֪��2KMnO4+5H2C2O4+3H2SO4=K2SO4+2MnSO4+10CO2��+8H2O��
�������Ʒ�в��ᾧ����H2C2O4��2H2O ����������������д�����������
[�й����ʵ���Է���������Mr��H2C2O4��=90��Mr��H2C2O42H2O��=126��Mr��KMnO4��=158 ]