题目内容
【题目】下图中的A是锶元素在元素周期表中的信息;B、C是与锶元素有关的粒子结构示意图。
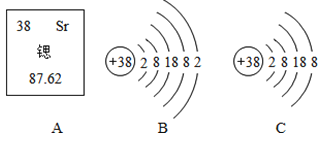
(1)锶元素的相对原子质量是________________;
(2)锶离子的符号是____________;
(3)元素在元素周期表中的周期数与其原子的核外电子层数相同,则锶元素在元素周期表中应排在第_____________周期。
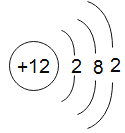
(4)电子距离原子核越远,越不易被束缚,越容易被失去。已知镁的原子结构示意图,推测镁和锶两种金属化学性质比较活泼的是________________。
【答案】87.62 Sr2+ 五 锶或Sr
【解析】
(1)由元素周期表中小方格中的信息可知锶元素的相对原子质量是87.62;
(2)由锶离子的结构示意图,每个锶离子带两个单位的正电荷,根据离子符号的书写规则,锶离子的符号是Sr2+;
(3)周期数与电子层数相同,锶原子核外有5个电子层,故锶元素在元素周期表中应排在第五周期;
(4)锶元素和镁元素的最外层电子数相等,但锶元素的原子核外电子层较多,最外层电子距离原子核更远,更容易被失去最外层两个电子,因此锶的化学性质比镁的活泼。

【题目】工业铁红可用于生产颜料,其主要成分是 Fe2O3,还含有少量的FeO、Fe3O4。为了测定某种工业铁红样品中铁元素的质量分数,同学们进行了如下探究。
(查阅资料)
Ⅰ.草酸晶体(H2C2O43H2O)在浓硫酸的催化下受热分解,会生成二氧化碳、一氧化碳和水。
Ⅱ.碱石灰是固体NaOH和CaO的混合物,能吸收水蒸气和二氧化碳
Ⅲ.铁的常见氧化物中,铁元素的质量分数如下表所示:
铁的氧化物 | FeO | Fe2O3 | Fe3O4 |
铁元素的质量分数 | 77.8% | 70.0% | 72.4% |
(设计与实验)小组同学设计了下图所示实验装置:
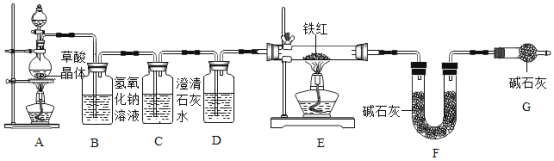
(1)为了保证进入E 中的气体是纯净、干燥的 CO,则 D 中的试剂名称为_____。
(2)C 装置的作用是_____。
(3)写出E 装置中发生反应的化学方程式(一个即可):_____。
(4)同学们称取 10.0g 铁红样品进行实验,根据资料信息推算,理论上铁红样品中铁元素质量的取值范围是_____。利用上述装置进行实验(装置气密性良好),并通过以下两种方法得出测定结果。
方法一:充分反应后,称量E 中得到的铁粉的质量,经计算求出铁元素的质量分数。
方法二:分别称量实验前后_____(填字母序号)装置的质量,经计算求出铁元素的质量分数。
(实验反思)
(1)如果缺少G 装置(不考虑其他因素),可能会导致利用方法二测定的样品中铁元素的质量分数偏小,原因是_____。
(2)从绿色化学的角度考虑,该实验装置的不足之处是_____。