题目内容
【题目】掌握化学实验中常用仪器的特征和用途,有利于开展化学学习和研究。现有下列仪器可供选择,回答下列问题(填序号)。
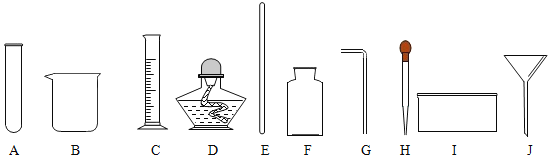
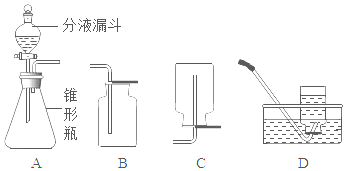
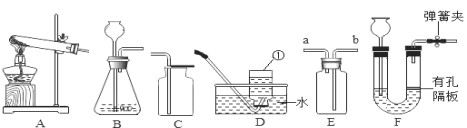
(1)可用作少量试剂的反应容器且能直接在酒精灯上加热的玻璃仪器是______;
(2)用于量取液体药品但不能用作反应容器的玻璃仪器是______;
(3)用于收集或贮存气体的玻璃仪器是______;
(4)用于吸取和滴加少量液体药品的仪器是______。
【答案】A C F H
【解析】
(1)可用作少量试剂的反应容器且能直接在酒精灯上加热的玻璃仪器是试管,故本题选A;
(2)用于量取液体药品但不能用作反应容器的玻璃仪器是量筒,故本题选C;
(3)用于收集或贮存气体的玻璃仪器是集气瓶,故本题选F;
(4)用于吸取和滴加少量液体药品的仪器是胶头滴管,故本题选H。

 新题型全程检测期末冲刺100分系列答案
新题型全程检测期末冲刺100分系列答案【题目】空气中氧气含量测定的再认识
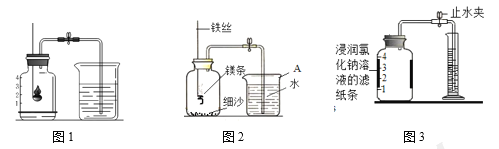
Ⅰ. 用红磷测定空气中氧气的含量。
(1)请写出红磷在空气中燃烧的化学表达式________。
(2)如图1所示进行实验, 测得空气中氧气的含量小于1∕5,可能的原因是 ____(填序号)。
A.燃烧匙伸入集气瓶太慢 B.红磷量不足
C. 实验中发现导管口有气泡冒出 D.装置漏气
Ⅱ. 用镁条测定空气中氧气的含量。
(3)请写出镁条在氧气中燃烧的化学表达式_____________。
(4)某同学利用图2实验测定空气中氧气含量时发现,产物中还出现少许黄色固体。
已知:镁能与氮气反应生成淡黄色的氮化镁(Mg3N2)固体。 但在空气中燃烧镁条时很难观察到生成物中有淡黄色固体,原因是_________。在操作规范的情况下,该同学实验所测得的氧气体积分数______1/5(填“大于”、“小于”或“等于”)。
Ⅲ. 用铁粉测定空气中氧气的含量。
(5)已知铁常温下与空气中的氧气、水反应生成铁锈(主要成分是Fe2O3﹒xH2O)。试写出该反应的化学表达式________。
(6)某同学根据铁生锈的原理,用铁粉测定空气中氧气的含量,设计了如图实验,8分钟后测得数据如表:
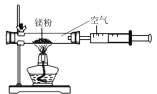
实验前的体积 | 实验后的体积 | |
集气瓶内空气 | 量筒内水 | 量筒内剩余水 |
250mL | 180.0mL | 129.5mL |
实验时该同学不是将铁粉堆在瓶底,而是将铁粉撒在浸润了氯化钠溶液的滤纸条上,再把该滤纸条贴在广口瓶内侧,其目的是________。根据表中数据计算得出空气中氧气的体积分数为________(结果保留到0.1%)。与用红磷燃烧的方法相比,用该方法测定空气中氧气的含量的主要优点一是没有污染,二是 ____________。
Ⅳ.拓展应用
(7)取2.4g镁条在O2和N2的混合气体中完全燃烧,所得固体质量为ag,,则a的取值范围是________g<a g<4g(结果保留到0. 1g)。
(8)已知:Fe2O3固体在一定的高温下能分解为一种复杂的铁的氧化物和一种气体。 该气体可以用___________来检验。现将64.0gFe2O3固体加热到该温度下,发现固体质量减少了3.2g后质量不再改变。请回答:64.0gFe2O3固体中含有铁元素_______g;该温度下复杂的铁的氧化物的化学式为__________。