题目内容
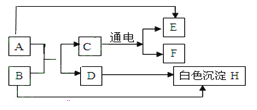
【题目】A-H是初中化学常见的物质,其相互转化关系如下图所示,其中A是人体胃液中帮助消化的物质,B是用于改良酸性土壤的碱。
(1)D的化学式为 。
(2)A与B反应的化学方程式为 _________,其反应基本类型属于 ; B转化为H的化学方程式为 ______________________ 。
(3)物质H的一种用途 。
【答案】(1)CaCl2 (2) Ca(OH)2 + 2HCl = CaCl2 + 2H2O 复分解反应
Ca(OH)2 + CO2 = CaCO3↓ + H2O (3) 建筑材料(或补钙剂或治疗胃酸过多)
【解析】
试题分析:框图式的推断题,抓住一些特殊的反应现象、特殊的性质及特殊的反应条件等级题目的“题眼”, 该题的题眼相对较多,A是人体胃液中帮助消化的物质,说明是盐酸;B是用于改良酸性土壤的碱,说明是氢氧化钙,C在通电情况下发生反应,说明是水,那么D自然为氯化钙
(1) D为氯化钙,化学式为:CaCl2
(2) A为盐酸,B为氢氧化钙,两者反应的化学方程式为:Ca(OH)2 + 2HCl = CaCl2 + 2H2O;反应基本类型属于复分解反应;B为氢氧化钙,H 为白色沉淀,可判断为碳酸钙,故B转化为H的化学方程式为:Ca(OH)2 + CO2 = CaCO3↓ + H2O
(3) 物质H为碳酸钙,它的一种用途:建筑材料(或补钙剂或治疗胃酸过多)

【题目】水和溶液在生命活动和生产、生活中起着十分重要的作用。请回答下列问题:
① 在水的净化过程中,常利用 (11) (填物质名称)的吸附性除去水中异味。净化过的水通入氯气后输送到每家每户,其中通入氯气的作用是 (12) 。
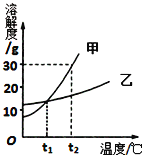
② 下表是NaOH和Ca(OH)2的溶解度数据(单位:g/100g水),请回答下列问题。
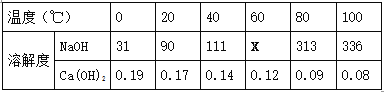
Ⅰ.表示溶解度的符号是 (13) ;表中“111”数字表示的含义是 (14) 。
Ⅱ.为测定X的值,取4份60℃的水各50克,分别进行实验,并记录数据如下表:
实验编号 | 实验1 | 实验2 | 实验3 | 实验4 |
NaOH质量/g | 50 | 60 | 70 | 80 |
H2O质量/g | 50 | 50 | 50 | 50 |
溶液质量/g | 100 | 110 | 114.5 | 114.5 |
【实验结果分析】实验1所得溶液的质量分数为 (15) ;由实验可知X的值为 (16) 。
Ⅲ.除去NaOH溶液中混有的少量Ca(OH)2,通过蒸发浓缩、 (17) ,然后过滤、洗涤、干燥得到NaOH固体。
Ⅳ.现有20℃时Ca(OH)2的饱和溶液(甲溶液),向其中加入一定量CaO后,恢复到原来温度得到的溶液(乙溶液),甲、乙溶液中溶质质量甲 (18) 乙(填“>、<、=”)。
Ⅴ.在20℃时,向盛有100g水的烧杯中加入111gNaOH,欲使其完全溶解变成不饱和溶液。下列说法中正确的是 (19) 。
A.溶液的质量可能不变 B.溶质的质量分数一定减小
C.溶液中溶质的质量一定增大 D.可以升温到40℃以上
E.NaOH的溶解度一定变大 F.20℃时加入的水的质量>23.4g
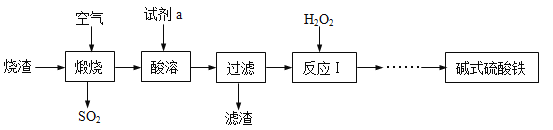
【题目】为比较相同浓度的FeCl3溶液和CuSO4溶液对H2O2分解的速率影响效果,某研究小组进行了如下探究:

【定性研究】
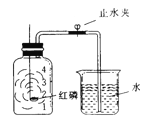
(1)如图甲,可通过观察_________________来定性比较两者的速率影响效果。
【定量研究】
(2)如图乙,实验前检查该装置气密性的方法是__________________________。要定量比较两者的速率影响效果,可测量生成等体积气体所需的_______________。
【深入研究】
(3)在FeCl3溶液中,究竟是哪种粒子影响过氧化氢的分解速率?
猜想1:水分子(H2O)影响过氧化氢的分解速率;
猜想2:___________影响过氧化氢的分解速率;
猜想3:___________影响过氧化氢的分解速率;……
请设计实验,验证猜想
实验操作 | 实验现象 | 实验结论 |
分别取同温度同体积同浓度的H2O2溶液于2支试管中,再分别加入等质量的FeCl3和NaCl。观察现象。 | 加入FeCl3的试管中产生的气体快,加入NaCl的试管中产生的气体慢。 | 证明是Fe3+影响过氧化氢的分解速率 |
(4)【反思与讨论】上述实验确实可以证明Fe3+可以改变过氧化氢的分解速率,但不能证明FeCl3是过氧化氢分解的催化剂。若要证明FeCl3是过氧化氢分解的催化剂,还需要通过实验证明FeCl3在反应前后 ___________________ 。
请写出FeCl3催化H2O2分解的化学方程式___________________________________。