题目内容
科学兴趣小组想研究影响过氧化氢(H2O2)分解速度的因素.在四支试管中分别加入0.2克二氧化锰(MnO2)粉末,然后加入等量的不同溶质质量分数的过氧化氢溶液,观察气泡产生的速度,记录如下:| 实验次数 | 1 | 2 | 3 | 4 |
| H2O2溶液的溶质质量分数 | 1% | 5% | 10% | 15% |
| MnO2质量 | 0.2克 | 0.2克 | 0.2克 | 0.2克 |
| 气泡产生的速率 | + | ++ | +++ | ++++ |
(2)该实验研究的问题是:过氧化氢分解的速率与 有关系,能得出的结论是 .
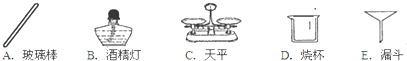
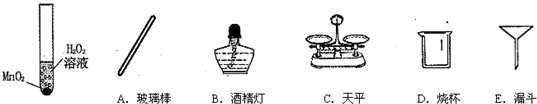
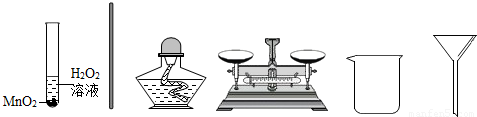
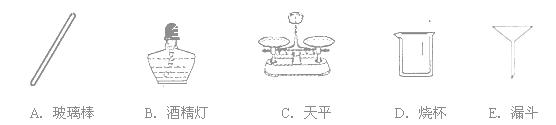
(3)实验完毕,可利用过滤法回收剩余溶液中的二氧化锰粉末.在过滤过程中,下列仪器不需要的有 .(填下列仪器名称)
【答案】分析:(1)根据制取氧气的原理及二氧化锰在该实验中起催化作用进行解答;
(2)根据实验中所给数据对比考虑解答并得出结论;
(3)根据过滤操作需要的仪器考虑.
解答:解:(1)用过氧化氢溶液在二氧化锰的作用下产生水和氧气,二氧化锰在该实验中加快了过氧化氢反应放出氧气的速率,但本身的质量和化学性质不变,二氧化锰在此实验中的作用是催化作用;其中的反应物是一种,生成物是两种,故是分解反应;
(2)由题目中的数据可知,在二氧化锰的量一定的情况下,双氧水溶液的溶质质量分数越大,气泡产生的速度越快,所以该实验研究的问题是过氧化氢分解的速度与双氧水溶液的溶质质量分数的关系;能得出的结论是:在二氧化锰一定时,过氧化氢溶液的溶质质量分数越大,则反应速率越快;
(3)过滤中用到的仪器:玻璃棒、烧杯、漏斗、铁架台等;而不需要天平和酒精灯;
故答案为:(1)催化作用、分解; (2)溶质质量分数;在二氧化锰一定时,过氧化氢溶液的溶质质量分数越大,则反应速率越快;(3)酒精灯、托盘天平.
点评:通过回答本题知道了影响过氧化氢反应速度的因素以及过滤中的注意事项.通过操作对比实验,在分析实验数据的基础上得到正确结论,是对学生分析能力的考查.
(2)根据实验中所给数据对比考虑解答并得出结论;
(3)根据过滤操作需要的仪器考虑.
解答:解:(1)用过氧化氢溶液在二氧化锰的作用下产生水和氧气,二氧化锰在该实验中加快了过氧化氢反应放出氧气的速率,但本身的质量和化学性质不变,二氧化锰在此实验中的作用是催化作用;其中的反应物是一种,生成物是两种,故是分解反应;
(2)由题目中的数据可知,在二氧化锰的量一定的情况下,双氧水溶液的溶质质量分数越大,气泡产生的速度越快,所以该实验研究的问题是过氧化氢分解的速度与双氧水溶液的溶质质量分数的关系;能得出的结论是:在二氧化锰一定时,过氧化氢溶液的溶质质量分数越大,则反应速率越快;
(3)过滤中用到的仪器:玻璃棒、烧杯、漏斗、铁架台等;而不需要天平和酒精灯;
故答案为:(1)催化作用、分解; (2)溶质质量分数;在二氧化锰一定时,过氧化氢溶液的溶质质量分数越大,则反应速率越快;(3)酒精灯、托盘天平.
点评:通过回答本题知道了影响过氧化氢反应速度的因素以及过滤中的注意事项.通过操作对比实验,在分析实验数据的基础上得到正确结论,是对学生分析能力的考查.

练习册系列答案
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案
相关题目
科学兴趣小组想研究影响过氧
化氢(H2O2)分解速度的因素。在四支试管中分别加入0.2克二氧化锰 (MnO2)粉末,然后加入等量的不同溶质质量分数的过氧化氢溶液,观察气泡产生的速度,记录如下:
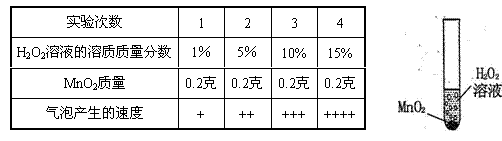 |
(1)该实验研究的问题是:过氧化氢分解的速度与_________的关系。 .
(2)为了检验产生的气体是否为氧气,请你写出检验的方法:____________________。
(3)实验完毕,可利用过滤法回收剩余溶液中的二氧化锰粉末。在过滤过程中,![]() 下列仪器不需要的有______________。
下列仪器不需要的有______________。
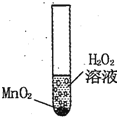 科学兴趣小组想研究影响过氧化氢(H2O2)分解速度的因素.在四支试管中分别加入0.2g二氧化锰
科学兴趣小组想研究影响过氧化氢(H2O2)分解速度的因素.在四支试管中分别加入0.2g二氧化锰 
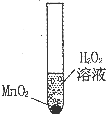 科学兴趣小组想研究影响过氧化氢(H2O2)分解速度的因素.在四支试管中分别加入0.2克二氧化锰 (MnO2)粉末,然后加入等量的不同浓度的过氧化氢溶液,观察气泡产生的速度,记录如下:
科学兴趣小组想研究影响过氧化氢(H2O2)分解速度的因素.在四支试管中分别加入0.2克二氧化锰 (MnO2)粉末,然后加入等量的不同浓度的过氧化氢溶液,观察气泡产生的速度,记录如下: