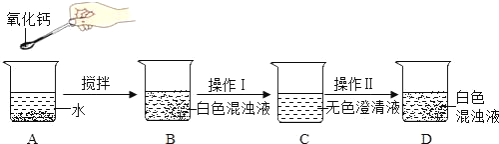
题目内容
【题目】某同学将一小包铜粉和锌粉的混合物放入一定量的硝酸银溶液中,使其充分反应后过滤,得到固体和蓝色滤液。并对滤液的组成进行探究。
(1)请写出一个相关反应的化学方程式。________
(2)同学们又对滤液中所含的物质作出多种猜想,有两种猜想可能成立,第一种猜想是滤液中含硝酸锌、硝酸铜,则另一种猜想应是什么?________
(3)请你设计实验方案来验证第一种猜想。________
【答案】 Zn+2AgNO3![]() Zn(NO3)2+2Ag或Cu+2AgNO3
Zn(NO3)2+2Ag或Cu+2AgNO3![]() Cu(NO3)2+2Ag 滤液中含AgNO3、Zn(NO3)2、Cu(NO3)2。 取样品少量,加入稀盐酸,无现象,证明溶液中没有AgNO3,只含Zn(NO3)2、Cu(NO3)2。
Cu(NO3)2+2Ag 滤液中含AgNO3、Zn(NO3)2、Cu(NO3)2。 取样品少量,加入稀盐酸,无现象,证明溶液中没有AgNO3,只含Zn(NO3)2、Cu(NO3)2。
【解析】(1)根据锌的活动性比银强,利用锌与硝酸银的反应规律,写出反应的化学方程式;(2)根据三种金属的活动性顺序锌铜银,推断将一小包铜粉和锌粉的混合物放入一定量的硝酸银溶液中可能发生的反应,得到固体和蓝色溶液,对反应后溶液的组成进行猜测;(3)根据三种金属活动性及氯离子与银离子不能共存的反应规律,设计验证猜想一。(1)锌置换硝酸银中的银,同时得到硝酸锌,反应的化学方程式为Zn + 2AgNO3 = Zn(NO3)2 + 2Ag;(2)由得到溶液呈蓝色,说明铜粉与硝酸银发生了反应,反应后溶液中一定含有硝酸铜;由于锌的活动性比铜强,锌会先于铜与硝酸银反应且锌粉可与硝酸铜反应,因此可判断锌粉已完全反应,溶液中一定含有硝酸锌;硝酸银是否完全反应则成为所要猜测的两种可能,若硝酸银完全反应,则溶液中只含有硝酸锌、硝酸铜,若硝酸银有剩余,则溶液中含有硝酸锌、硝酸铜、硝酸银(或AgNO3、 Zn(NO3)2、 Cu(NO3)2);(3)取样品少量,加入稀盐酸,无现象,证明溶液中没有AgNO3,因为溶液呈蓝色,所以一定有Cu(NO3)2,Zn和AgNO3反应生成了Zn(NO3)2,所以溶液中只有Zn(NO3)2、 Cu(NO3)2,没有AgNO3。

【题目】化学小组受英国科学家法拉第《蜡烛的化学史》的启发,对蜡烛的燃烧过程进行了再一次探究。

【查阅资料】
硫酸铜(CuSO4)是一种白色粉末,易吸水,吸水后变为蓝色。
【进行实验】
序号 | 实验步骤 | 实验现象 | 实验结论 |
I |
| 外焰处的铁纱网出现红热的环,内焰及焰心处的铁纱网无明显变化 | |
II |
| 伸入焰心的导气管引出白烟, | 焰心处有可燃性气体 |
III |
| 蜡烛燃烧的产物中有水和二氧化碳 |
(1)实验I得到的结论是_________________________________________________。
(2)补全实验II的实验现象______________________________________________。
(3)实验III中,硫酸铜粉末的作用是___________________;得到“蜡烛燃烧的产物中含有二氧化碳”这一结论所对应的实验现象是___________________________。
(4)依据实验III,可以得到关于蜡烛的元素组成情况是________________________。
【反思与评价】
(5)实验III是该小组同学对右图所示实验的改进。与右图所示实验相比,实验3的优点是______。