题目内容
【题目】下图是某同学对二氧化碳部分知识构建的网络图(部分反应条件和部分生成物省略)。按下列要求填空:
(1)写出a燃烧的化学方程式。
(2)物质d的化学式是。
(3)二氧化碳转化为C属于变化(填“物理”或“化学”)。
(4)固体二氧化碳称为 , 可用于人工降雨。
(5)二氧化碳过多会引起温室效应,有研究指出可用地下盐水储存CO2 , 此过程中涉及到反应2Mg2SiO4+2H2O+CO2═Mg3Si2O5(OH)4+ X ,则生成物X 为(填化学式)。
(6)含碳物质燃烧会污染空气,研制和开发不含碳并可用于工业生产的清洁能源,一直是科学家不懈追求的目标。氨气(NH3)在空气中充分燃烧的产物是氮气和水,目前液氨被人们称为一种潜在的清洁燃料。
液氨和液氢燃料相比有关数据见下表,据此判断不正确的是__________(填序号)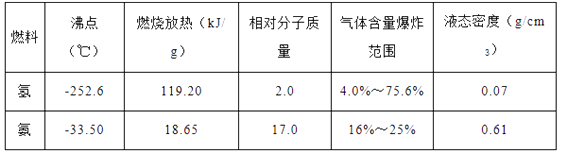
A.氨泄漏到空气中比氢气更易发生爆炸
B.以氨和氢为燃料时,可以减缓温室效应
C.氨的液化比氢气容易得多
D.等质量的氨和氢分别燃烧,氢放出的热量多
【答案】
(1)CH4 + 2O2 ![]() CO2 +2 H2O
CO2 +2 H2O
(2)H2CO3
(3)化学
(4)干冰
(5)MgCO3
(6)A
【解析】(1) 天然气的主要成分是甲烷,燃烧的化学方程式:CH4 + 2O2 ![]() CO2 +2H2O;(2)二氧化碳和水反应生成碳酸,化学式是H2CO3;(3)二氧化碳转化为葡萄糖,物质的种类改变,属于化学变化;(4)固体二氧化碳称为干冰,可用于人工降雨;(5) 据质量守恒定律可知,化学反应前后原子的种类、个数不变;依据2Mg2SiO4+2H2O+CO2═Mg3Si2O5(OH)4+ X ,则生成物X 为MgCO3;(6) A.由表格中的数据可知,氨气的爆炸极限范围远远小于氢气的爆炸极限范围,所以氨气泄漏到空气中比氢气难发生爆炸 ,错误; B.以氨气和氢气为燃料时,生成物中没有二氧化碳,可以减缓温室效应,正确;C.氨气的沸点比氢气的高很多,所以液化比氢气容易得多,正确; D.氢气的热值比氨气高,等质量的氨和氢分别燃烧,氢放出的热量多,正确。故选A。
CO2 +2H2O;(2)二氧化碳和水反应生成碳酸,化学式是H2CO3;(3)二氧化碳转化为葡萄糖,物质的种类改变,属于化学变化;(4)固体二氧化碳称为干冰,可用于人工降雨;(5) 据质量守恒定律可知,化学反应前后原子的种类、个数不变;依据2Mg2SiO4+2H2O+CO2═Mg3Si2O5(OH)4+ X ,则生成物X 为MgCO3;(6) A.由表格中的数据可知,氨气的爆炸极限范围远远小于氢气的爆炸极限范围,所以氨气泄漏到空气中比氢气难发生爆炸 ,错误; B.以氨气和氢气为燃料时,生成物中没有二氧化碳,可以减缓温室效应,正确;C.氨气的沸点比氢气的高很多,所以液化比氢气容易得多,正确; D.氢气的热值比氨气高,等质量的氨和氢分别燃烧,氢放出的热量多,正确。故选A。
所以答案是:CH4 + 2O2 ![]() CO2 +2 H2O;H2CO3;化学;干冰;MgCO3;A。
CO2 +2 H2O;H2CO3;化学;干冰;MgCO3;A。
【考点精析】本题主要考查了二氧化碳的化学性质和二氧化碳的用途的相关知识点,需要掌握化学性质:一般情况下不能燃烧,也不支持燃烧,不能供给呼吸;与水反应生成碳酸;能使澄清的石灰水变浑浊;与灼热的碳反应;用途:灭火;既利用其物理性质,又利用其化学性质;干冰用于人工降雨、制冷剂;温室肥料才能正确解答此题.

 超能学典应用题题卡系列答案
超能学典应用题题卡系列答案【题目】某实验小组的同学用氢氧化钠溶液和稀硫酸进行酸碱中和反应的实验时,向烧杯中的氢氧化钠溶液滴加稀硫酸一会儿后,发现忘记了滴加指示剂。此时,他们停止滴加稀硫酸,并对烧杯内溶液中溶质的成分进行探究。
(1)Ⅰ.写出该中和反应的化学方程式。
(2)Ⅱ.探究烧杯内溶液中溶质的成分:
【提出问题】该烧杯内溶液中溶质是什么?
【进行猜想】
猜想一:可能是Na2SO4与NaOH ;猜想二:可能只是Na2SO4 ;猜想三:可能是。
(3)【查阅资料】Na2SO4溶液呈中性。
【实验探究】
实验步骤 | 实验现象 | 实验结论 |
①取少量烧杯内溶液于试管中,滴入几滴酚酞溶液,振荡 | 猜想一不正确 | |
②取少量烧杯内溶液于另一支试管中,滴加碳酸钠溶液 | 猜想二不正确,猜想三正确 |
(4)【反思与拓展】
探究猜想三成立,除以上方案外,下列哪些物质也能完成该实验?(填序号)
A.pH试纸
B.铜
C.氧化铜
D.氢氧化铜
(5)甲、乙两位同学准备测定反应后溶液中H2SO4的质量分数。
①甲同学取50g该溶液于烧杯中,逐滴滴入溶质质量分数为10%的NaOH溶液,反应过程中溶液的pH变化如右图所示,求溶液中H2SO4的质量分数。(写出计算过程)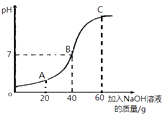
②试写出A点溶液中的溶质。
③乙同学改用BaCl2溶液代替NaOH溶液,根据生成沉淀的质量来确定溶液中H2SO4的质量分数,你认为结果将(填“偏大”“偏小”或“无影响”)。
【题目】人类社会发展离不开金属材料,结合所学知识,回答下列问题:
(1)生活中使用的金属材料大多是合金,而不是纯金属,这是因为合金具有更多性能。例如,钢比纯铁硬度__________(填“大”或“小”)。下列属于合金的是_____(填字母序号)。
a.黄铜 b.铝 c.生铁
(2)铁是化学性质比较活泼的金属,它在自然界主要以_________(填“单质”或“化合物”)的形式存在,为了防止铁栏生锈可采取的措施是_________________。
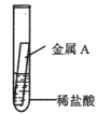
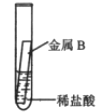
(3)某学习小组在学习金属的化学性质时,进行如下实验:
实验操作 | | |
实验现象 | 金属表面产生气泡 | 金属表面无明显现象 |
由实验可知,两种金属的活动性顺序是A__________B(填“>”或“<”),若金属A为铁,则反应的化学方程式为_____________。