题目内容
【题目】M是生活中常见的金属,MSO4溶液是无色液体,某化学兴趣小组的同学欲探究M与铜、铝的活动性顺序,请你和他们一起进行以下探究活动。
(提出问题)M、铜、铝的金属活动性顺序是怎样的?
(猜想与假设)小敏的猜想是Al>Cu>M;小强的猜想是Al>M>Cu;你的猜想是_____。
(设计与实验)为了探究三种金属的活动性顺序,同学们取粗细相同的M丝、铝丝及相关溶液,进行了如图所示的实验:
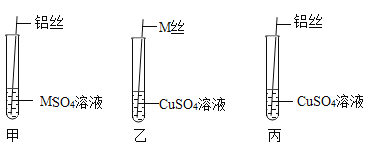
观察到只有试管乙中发生明显变化,那么试管乙中观察到的现象是________。
(交流与表达)(1)同学们一致认为试管丙中也应该有明显变化,之所以出现这种情况的原因可能是_____________。
(2)于是同学们对实验进行了改进,把甲、丙中的铝丝打磨干净后又分别插入原试管中,结果甲、丙试管中都出现了明显变化,则丙试管中发生反应的化学方程式为__________。
(解释与结论)通过以上实验,同学们得出了三种金属的活动性顺序。
(评价与反思)实验结束后,同学们对实验过程进行了如下反思:
(1)同学们经过讨论后认为该实验可以优化,去掉试管_______(填试管编号)中的实验,也可以得出正确的结论。
(2)除了上述实验外,还可以将铝丝、铜丝分别插入到盛有___________溶液的试管中,或将___________(填一种物质)分别插入到硫酸铝、硫酸铜溶液中,根据实验现象进行判断。
【答案】M>Al>Cu M表面出现一层红色物质 铝丝表面有氧化铝保护膜阻止反应的进行 2Al+3CuSO4=Al2(SO4)3+3Cu 丙 MSO4 M丝
【解析】
[提出问题]通过分析小敏、小强同学的猜想可知,我的猜想是M>Al>Cu;故填:M>Al>Cu;
[设计与实验]M的金属活动性大于铜的金属活动性,所以试管乙中观察到的现象是:M表面出现一层红色物质;故填:M表面出现一层红色物质;
[交流与表达](1)试管丙中使用的是铝丝,没有明显变化可能是因为铝丝表面有氧化铝保护膜阻止反应的进行,故填:铝丝表面有氧化铝保护膜阻止反应的进行。
(2)丙试管中铝与硫酸铜反应生成硫酸铝和铜,发生反应的化学方程式为,故填:2Al+3CuSO4=Al2(SO4)3+3Cu。
[评价与反思](1)可以去掉试管丙中的实验,得出正确的结论,故填:丙。
(2)要验证三种金属的活动性顺序,可以采用三取其中的方法,故除了上述实验外,还可以将铝丝、铜丝分别插入到盛有MSO4溶液的试管中,或将M丝分别插入到硫酸铝、硫酸铜溶液中。故填:MSO4;M丝。

 阅读快车系列答案
阅读快车系列答案【题目】根如据图所示装置完成实验,并按要求填写表格内容。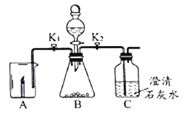
关闭K2打开K1A中现象 | B中发生反应化学方程式 | 解释A中现象 | 关闭K1打开K2C中现象 | 用化学方程式解释C中现象 |
蜡烛熄灭 | ______ | _____ | _____ | _____ |
蜡烛燃烧更旺 | _____ | ______ | _____ |