题目内容
【题目】某化学兴趣小组为测定某石灰石样品中碳酸钙的质量分数,取40克石灰石样品放在烧杯中,然后向其中逐滴加入稀盐酸,使之与稀盐酸充分反应(杂质不参与反应),恰好完全反应时,加入稀盐酸的质量为200克,反应后烧杯中物质的总质量为226.8克。请计算:
(1)反应生成二氧化碳的质量_________。
(2)石灰石样品中碳酸钙的质量分数_________。
【答案】13.2g 75%
【解析】
(1)根据反应前后物质质量的变化可计算出生成的二氧化碳的质量,反应生成的二氧化碳的质量=40g+200g-226.8g=13.2g;
故填:13.2g。
(2)根据(1)所计算的二氧化碳,根据化学方程式的计算,首先算出碳酸钙的质量,再根据![]() ,计算出样品中碳酸钙的质量分数。
,计算出样品中碳酸钙的质量分数。
设生成13.2g二氧化碳需要碳酸钙的质量为x

![]()
解得:x=30g
石灰水样品中碳酸钙的质量分数为:![]() 。
。
答:(1)反应生成的二氧化碳的质量是13.2g;
(2)石灰石样品中碳酸钙的质量分数是75%。

【题目】下图甲是氢气和氧化铜反应的实验装置,下图乙是木炭和氧化铜反应的实验装置。
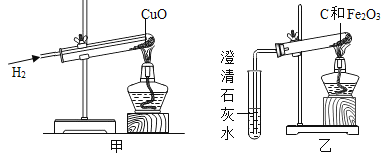
(1)在上述两个实验中,氢气和木炭表现出相同的化学性质,该化学性质是____________。
(2)实验操作的准确是实验成功的关键,甲实验中,反应前必须先通氢气后点燃酒精灯,否则易发生______________;乙实验中,若要观察到理想的现象,需要做的装置改进是____________________。
(3)按图乙中原装置做完实验后,观察到小试管中澄清石灰水变浑浊,大试管中粉末全部变为红色;老师却指出,此时产生的红色固体成分还需要进一步研究:
【提出问题】木炭与氧化铜反应生成的红色固体中可能含有什么物质?
【查阅资料】木炭与氧化铜反应也可能生成氧化亚铜(Cu2O);氧化亚铜是红色固体,能与稀硫酸反应:Cu2O+H2SO4=Cu+CuSO4+H2O。
【进行猜想】木炭与氧化铜反应生成的红色固体成分:
①_________________;②全部是氧化亚铜;③是两者的混合物。
【实验探究】
步骤 | 现象 | 结论 |
取1.8g红色固体于试管中,滴加足量________,充分反应 | _____________________ | 猜想①错误 |
过滤,将滤渣洗涤、干燥、称量 | 所得固体质量范围为_______ | 猜想③正确 |