题目内容
【题目】“空气中氧气含量测定”再研究
【回顾历史】1774年,某科学家通过用金属汞在空气中加热生成氧化汞等实验,第一次明确得出空气是由氧气和氮气组成的结论。
(1)上文中这位科学家是 (____________)
A.诺贝尔 B.居里夫人 C.门捷列夫 D.拉瓦锡
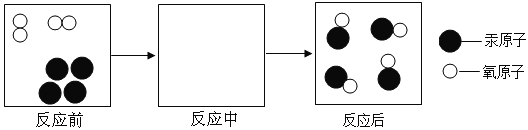
(2)以下微粒示意图可简单表示金属汞与氧气反应的过程,请在反应中方框内画出正确的图示 (____________)。
【重温教材】实验室常用红磷燃烧的方法测定空气中氧气的含量(装置如下图),写出反应的符号表达式___________________。理论上实验成功时的现象是:_____________。实际上用该方法测得的氧气含量常常远低于理论值。
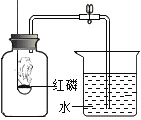
【提出问题】实验中装置内部的情况是怎样的,用红磷燃烧的方法为什么不能准确地测定空气中氧气的含量?
【进行实验】查阅资料后,学习小组进行如下实验:
(1)将数显设备(电脑等)、三种传感器(压强、温度、O2浓度)、测量装置(反应容器为蒸馏水瓶)按下图所示进行连接。
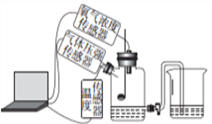
(2)打开导管活塞,向烧杯内加入适量的水,双手紧贴蒸馏水瓶外壁,_____________,则说明装置气密性良好。
(3)打开瓶口橡皮塞,加水并调节使蒸馏水瓶和烧杯内液面相平,关闭活塞,打开并调试好传感器和数显设备。用酒精灯将足量的红磷点燃,立即将燃烧匙伸入瓶中并赛紧橡皮塞
(4)燃烧结束后,装置冷却到室温,打开导管活塞,待瓶内液面不再上升后再向烧杯内加入一定量的水,使烧杯和瓶内的液面相平。在数显设备上得到的曲线图(纵坐标为O2浓度,横坐标为时间,压强和温度曲线仅表示该段时间内对应的变化情况)如下图所示
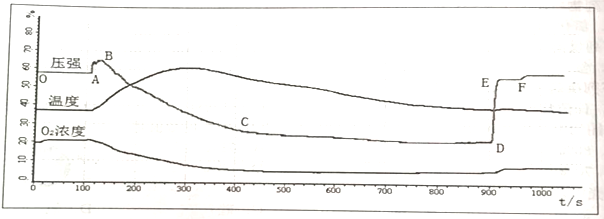
【数据分析】
(1)压强曲线A点表示红磷开始在集气瓶中燃烧,主要判断依据是:____________;
(2)压强曲线CD段降低的原因是___________________________;
(3)压强曲线EF段略低于OA段是因为________________________________;
【实验结论】用红磷燃烧的方法不能准确测定空气中氧气含量的原因是_______________;
【反思拓展】甲同学认为应该将蒸馏水瓶液面上的容积划分为5等分并加以标记,乙同学认为没有必要,理由是__________________________________________。
【答案】 D 图略 略 打开止水夹后水进入集气瓶占集气瓶容积的五分之一 导管口有气泡冒出,松手后导管内侧吸形成一段水柱 A点对应的氧气浓度开始降低 温度下降(装置冷却) 烧杯内液面低于蒸馏水瓶中液面(烧杯和蒸馏水瓶中液面不相平) 红磷燃烧不能将空气中的氧气耗尽 氧气的体积含量可在数显设备上直接显示(或氧气的体积含量可根据压强变化数值计算)
【解析】【回顾历史】(1) 1774年,拉瓦锡通过用金属汞在空气中加热生成氧化汞等实验,第一次明确得出空气是由氧气和氮气组成的结论;(2)根据质量守恒定律,反应中原子的个数、种类不变,可推知:  ;【重温教材】红磷燃烧生成五氧化二磷,反应的符号表达式为:磷+氧气
;【重温教材】红磷燃烧生成五氧化二磷,反应的符号表达式为:磷+氧气![]() 五氧化二磷,当打开止水夹后水进入集气瓶占集气瓶容积的五分之一说明实验成功了; 【进行实验】(2) 打开导管活塞,向烧杯内加入适量的水,双手紧贴蒸馏水瓶外壁,导管口有气泡冒出,松手后导管内侧吸形成一段水柱,则说明装置气密性良好;【数据分析】 (1)红磷开始在集气瓶中燃烧时,氧气开始消耗,A点对应的氧气浓度开始降低; (2)红磷燃烧消耗完氧气后,装置冷却,导致瓶内压强减小; (3)红磷燃烧消耗完氧气后,装置冷却后,水会从烧杯进入集气瓶内,会导致烧杯内液面低于蒸馏水瓶中液面(烧杯和蒸馏水瓶中液面不相平) ;【实验结论】过量的红磷燃烧消耗氧气,不能将氧气全部消耗尽;【反思拓展】此装置连接着数据分析系统,实验结束后,氧气的体积含量可在数显设备上直接显示(或氧气的体积含量可根据压强变化数值计算) 。
五氧化二磷,当打开止水夹后水进入集气瓶占集气瓶容积的五分之一说明实验成功了; 【进行实验】(2) 打开导管活塞,向烧杯内加入适量的水,双手紧贴蒸馏水瓶外壁,导管口有气泡冒出,松手后导管内侧吸形成一段水柱,则说明装置气密性良好;【数据分析】 (1)红磷开始在集气瓶中燃烧时,氧气开始消耗,A点对应的氧气浓度开始降低; (2)红磷燃烧消耗完氧气后,装置冷却,导致瓶内压强减小; (3)红磷燃烧消耗完氧气后,装置冷却后,水会从烧杯进入集气瓶内,会导致烧杯内液面低于蒸馏水瓶中液面(烧杯和蒸馏水瓶中液面不相平) ;【实验结论】过量的红磷燃烧消耗氧气,不能将氧气全部消耗尽;【反思拓展】此装置连接着数据分析系统,实验结束后,氧气的体积含量可在数显设备上直接显示(或氧气的体积含量可根据压强变化数值计算) 。

 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案【题目】课外兴趣小组选择“H2O2 生成O2 的快慢与什么因素有关”的课题进行探究,以下是他们探究的主要过程:
(1)【假 设】1、H2O2 生成O2 的快慢与催化剂种类有关
【实验方案】常温下,在两瓶同质量、同浓度的H2O2 溶液中,分别加入相同质量的MnO2 和水泥块,测量各生成一瓶(相同体积)O2 所需的时间。
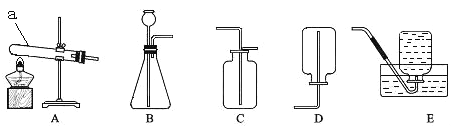
(2)【进 行 实 验】下图是他们进行实验的装置图。请写出过氧化氢在二氧化锰的催化下发生反应的符号表达式________________________________。在B位置最好选用_________ 法来收集氧气(选填“向上排空气法”或“排水法”),长劲漏斗下端管口应插在______(选填“液面上”或“液面下”)。
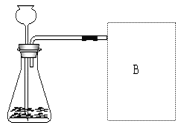
(3)【 实验记录】
实验编号 | 1 | 2 |
反应物 | 5%H2O2 | 5%H2O2 |
催化剂 | 1g水泥块 | 1gMnO2 |
时间 | 165秒 | 46秒 |
(4)【 结 论】该探究过程得出的结论是__________________________________。
(5)【 反 思】H2O2在常温下分解缓慢,加入MnO2或水泥块后反应明显加快,若要证明MnO2和水泥块是该反应的催化剂,还需要增加实验来验证它们在化学反应前后的 ____________________是否改变。
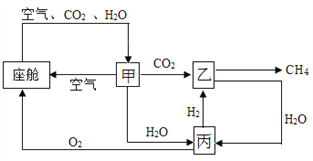
【题目】碳家族是是化学世界里最大的家族,一直受到人们关注。
(1)甲烷(CH4)— 最简单的含碳化合物。
①化学家在较低的温度和压力下,用甲烷等为原料制成了金刚石薄膜,该变化属于_____(填“物理变化”或‘化学变化”)。
②已知在相同条件下,相同体积的气体所含的分子数目相同,CO、CH4燃烧的化学方程式分别为:2CO+O2![]() 2CO2;CH4+2O2
2CO2;CH4+2O2![]() CO2+2H2O。据此分析,在相同条件下,分别燃烧1米3的CO和1米3的CH4,消耗氧气的质量比是________________。
CO2+2H2O。据此分析,在相同条件下,分别燃烧1米3的CO和1米3的CH4,消耗氧气的质量比是________________。
③常温常压时,由甲烷和另两种气体组成的混合物中,碳元素的质量分数为80%,则另两种气体可能是__________(填字母序号)。
A.H2和C2H6 B.H2和C2H2 C.CO和C2H6 D.C2H2和C2H4
④甲烷和水反应后可以制成水煤气,其反应的微观示意图如下所示,根据微观示意图得出的结论中,正确的是_________(填字母序号)。
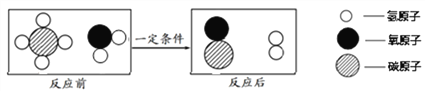
A.反应前后各元素的化合价均不变 B.反应后所得的水煤气是混合物
C.该反应中含氢元素的化合物有2种 D.该反应中分子的种类不变
(2)CO2 — 常见的含碳化合物
①造成大气中CO2含量增加的主要原因是________(填字母序号)。
A.动植物的呼吸作用 B.实验室逸出CO2 C.化石燃料的大量燃烧
②汽车尾气中的CO和NO,在催化剂作用下能转化为CO2和N2,该反应中CO和NO的分子个数比为________________。
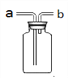
③实验室常用石灰石和稀盐酸制取二氧化碳,用下图装置检验气体是否是CO2,瓶内装入的物质是____________,若用右图装置收集CO2,CO2应从______通入。
④学校化学兴趣小组同学为测定本次实验中所用石灰石中碳酸钙的质量分数。称取一定质量的石灰石样品,把50g稀盐酸分5次加入样品中(假设杂质不反应也不溶解),得实验数据如下:
稀盐酸的用量 | 剩余固体的质量 |
第一次加入10g | 4.0g |
第二次加入10g | 3.0g |
第三次加入10g | 2.0g |
第四次加入10g | Xg |
第四次加入10g | 0.5g |
请计算:
Ⅰ.表中X的数值是______
Ⅱ.这种石灰石样品中碳酸钙的质量分数是______ 。
Ⅲ.这些样品完全反应共产生CO2的质量是______?(写出计算过程,结果精确到0.01g)