题目内容
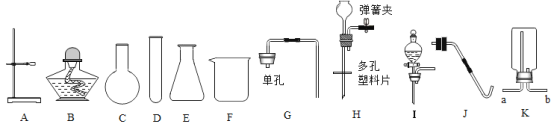
【题目】某学校环保实验小组的同学定期会对学校旁边的小河河水进行酸碱度及金属含量测定,其中操作不正确的是
A.定量量取河水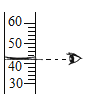 B.过滤河水泥沙
B.过滤河水泥沙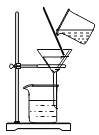 C.测定河水pH
C.测定河水pH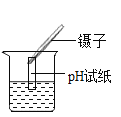 D.测定金属含量
D.测定金属含量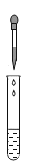
【答案】C
【解析】
A.量筒读数时,视线要与量筒内凹液面的最低处保持水平,A操作正确,不符合题意;
B.过滤操作的三个要点为“一贴二低三靠”,B操作用正确,不符合题意;
C.测定pH时,应将pH试纸置于干燥、洁净的玻璃片或表面皿或点滴板上,然后用干燥、洁净的玻璃棒蘸取(或胶头滴管吸取)少量待测液滴在pH试纸上,显色后与标准比色卡对比读数,不能直接将pH试纸伸入待测液中,否则会污染待测液,C操作不正确,符合题意;
D.用胶头滴管滴加液体时,胶头滴管应该竖直悬空于试管口的正上方,不能伸人试管中,D操作正确,不符合题意。
故选:C。

【题目】向盛有10mL NaOH溶液(其中滴有少量无色酚酞溶液)的烧杯中逐滴加入稀盐酸,用pH计(用来精确测定溶液pH的仪器)测定溶液的pH,所得数据如下:
加入稀盐酸的体积/mL | 0 | 2 | 4 | 6 | 8 | 10 | 12 | 14 |
烧杯中溶液的pH | 12.9 | 12.7 | 12.5 | 12.3 | 11.9 | 7.0 | 2.1 | 1.9 |
(1)当加入稀盐酸的体积为___________ mL时,NaOH溶液和稀盐酸恰好完全反应,反应的化学方程式为_____________。
(2)当加入稀盐酸的体积为3mL时,溶液显________色;
(3)当烧杯中溶液的pH=2.1时,溶液中的溶质有:__________________。
【题目】胃酸过多须服用抗酸药物(能与盐酸反应),常用的抗酸药物有碳酸氢钠片、铝碳酸镁片,兴趣小组的同学对这两种药物开展如下探究。
(查阅资料)①铝碳酸镁片的主要成分的化学式为AlMg(OH)3CO3;
②抗酸原理:抗酸药物中的离子和胃酸中的氢离子反应,降低胃液酸性。
活动一:定性探究抗酸药物与“胃酸”的反应。
(1)铝碳酸镁片中含有铝离子、镁离子、氢氧根离子和碳酸根离子。结合上述知识分析,该药物起抗酸作用的微粒是_____(填化学符号)。
(2)小王取一定量碳酸氢钠片与4mLpH═1的稀盐酸(模拟胃酸)反应。药片中其他成分不溶于水也不参加反应。他对反应后溶液的成分产生了兴趣。
(作出猜想)
猜想 1:只含 NaCl;
猜想 2:_____;
猜想 3:NaCl、NaHCO3
(设计实验)
实验步骤 | 实验现象 | 实验结论 | |
实验一 | 取一定量反应后的溶液于试管中,滴加_____ | 无明显现象 | 猜想 3错误 |
实验二 | 另取一定量反应后的溶液于试管中,______ | ______ | 猜想 2正确 |
实验二中涉及反应的化学方程式为______。
活动二:定量探究抗酸药物与“胃酸”的反应,对比分析产生 CO2的速率快慢和中和酸的能力强弱。
如图 1,利用数字化实验分别测定碳酸氢钠片、铝碳酸镁片与“胃酸”反应时,产生 CO2的速率快慢和 pH的变化,得到“二氧化碳浓度与时间”曲线(如图 2)、“pH与时间”曲线(如图 3)。
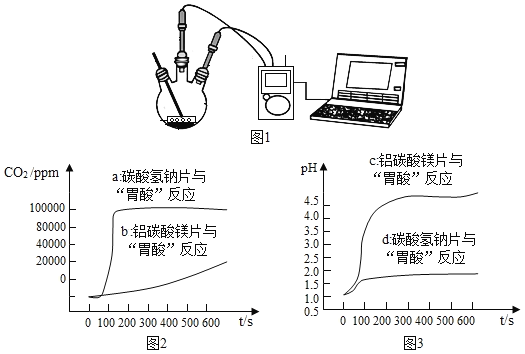
(1)服用碳酸氢钠片更易造成胃胀气,原因是_____。
(2)铝碳酸镁片中和酸的能力更强,理由是_____。
(反思与提升)日常生活中,我们应该根据个人的具体病情,选择合适种类的胃药。