题目内容
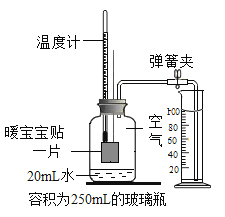
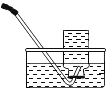
【题目】某化学小组通过如图所示装置,测定产生相同体积气体所用时间长短来探究影响过氧化氢分解速率的因素。
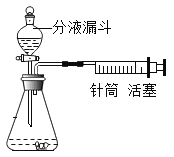
(1)简要说明如何检查如图装置的气密性_________________。
(2)实验探究
(设计实验)每次均用30mL10%的过氧化氛溶液,采用不同量的二氧化锰粉末作催化剂,测定各次收集到500mL氧气时所用的时间,结果如下:(其他实验条件均相同)
实验次序 | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 |
二氧化锰粉末用量/g | 0.1 | 0.2 | 0.3 | 0.4 | 0.5 | 0.6 | 0.7 | 0.8 | 0.9 | 1.0 |
所用时间/s | 17 | 8 | 7 | 5 | 4 | 3 | 2 | 2 | 2 | 2 |
(实验结论)请分析表中数据回答:二氧化锰的用量对反应速率有没有影响呢?__________(填“有”或“无”)。如果有,是怎样影响的呢?____________。
(拓展迁移)还有哪些因素可能影响该反应的速率呢?请说出你的一个猜想:_________。简要设计实验来证明你的猜想______________。
【答案】先关闭分液漏斗的活塞,用力将注射器的活塞向右拉动一段距离,然后松开,若活塞回到原来位置,则气密性良好 有 在一定范围内,随着二氧化锰质量的增加,过氧化氢溶液的分解速率增大,当二氧化锰的质量增大到一定的值,过氧化氢溶液的分解速率就不再随二氧化锰质量的增加而增大 过氧化氢溶液的质量分数 取5%和10%的过氧化氢溶液各30mL,分别加入0.8g二氧化锰,比较各收集250mL氧气需要时间的多少,得出过氧化氢溶液的质量分数大小对过氧化氢溶液分解速率影响的结论。
【解析】
(1)检查题中装置的气密性方法是:先关闭分液漏斗的活塞,用力将注射器的活塞向右拉动一段距离,然后松开,若活塞回到原来位置,则气密性良好。
(2)实验探究
实验结论:根据表中数据,二氧化锰的质量从0.1g逐渐增大到0.7g,收集500mL氧气所用的时间由17s减少到2s,可见二氧化锰的用量对反应速率有影响,但当二氧化锰的质量增大到0.7g后,继续增加二氧化锰的质量,收集同样多的氧气所需时间不再发生变化,因此影响的具体情况是:在一定范围内,随着二氧化锰质量的增加,过氧化氢溶液的分解速率增大,当二氧化锰的质量增大到一定的值,过氧化氢溶液的分解速率就不再随二氧化锰质量的增加而增大。
拓展迁移:影响该反应速率的因素除了上述二氧化锰的质量多少,还可能有:过氧化氢溶液的质量分数大小。
设计的实验方案是:取5%和10%的过氧化氢溶液各30mL,分别加入0.8g二氧化锰,比较各收集250mL氧气需要时间的多少,得出过氧化氢溶液的质量分数大小对过氧化氢溶液分解速率影响的结论。。

 互动英语系列答案
互动英语系列答案 名牌学校分层周周测系列答案
名牌学校分层周周测系列答案【题目】催化剂在化学反应中起着非常重要的作用,某兴趣小组进行如下探究。
探究一 催化剂的选择
研究表明,许多金属氧化物对氯酸钾有催化作用。分别用下列金属氧化物作催化剂,氯酸钾开始发生分解反应和反应剧烈时的温度如表所示:
温度 | Fe2O3 | Al2O3 | CuO | MgO |
开始反应 | 470 | 515 | 305 | 490 |
剧烈反应 | 490 | 540 | 350 | 545 |
(1)上述实验中,从温度对反应催化效果来看,最好选用__________作催化剂。
探究二 氧化铜与二氧化锰的催化效果进行比较
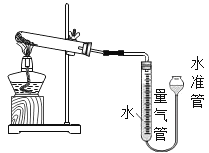
用如图装置进行实验,实验均以生成25mL气体为准,可能影响实验的因素均已忽略,相关装置和数据见下表:
序号 | KClO3质量 | 催化剂质量 | 待测试剂 |
① | 2.45g | — | a |
② | 2.45g | 0.51gMnO2 | b |
③ | 2.45g | 0.51gCuO | c |
(2)上述实验中的“待测数据”是________________。若b_________c(填“>”、“=”或“<”)可知在某温度下氧化铜对氯酸钾分解效果更好。
探究三 氧化铜与二氧化锰的对于过氧化氢的催化效果进行比较
安妮同学用如图1所示的装置进行了两次实验,在试管中分别加入等质量的氧化铜和二氧化锰,分别将注射器内盛有的双氧水注入试管中,利用注射器收集氧气,收集到氧气的体积和时间的关系如图2所示。
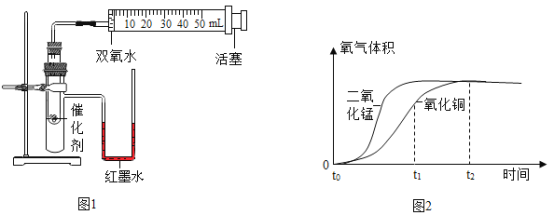
(3)装入药品前检查该装置气密性的方法是_____________,开始实验时注入双氧水的方法是________(填序号),另一种方法除了误差较大,还可能造成的后果是_____________。
A快速推注射器活塞 B缓慢推注射器活塞
(4)实验中造成U形管内红墨水液面左低右高的可能原因是_____________。
(5)通过图象2除了能得出二氧化锰催化效果比氧化铜好,还能得出的结论是________________。
(6)由氧化铜催化的反应,t1-t2时间段反应速率逐渐变_______(填“快”或“慢”),原因是___________________。
【题目】水在化学实验中有多种用途,对下列实验中水的作用解释不正确的是( )
A | B | C | D | |
实 验 装 置 |
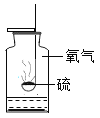
硫在氧气中燃烧 |
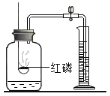
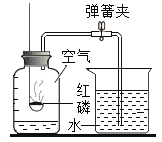
测定空气中氧气含量 |
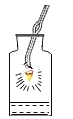
铁丝在氧气中燃烧 |
排水法收集氧气 |
作用 | 集气瓶中的水; 吸收热量,防止集气瓶炸裂。 | 量筒中的水: 通过体积变化得出 空气中氧气的体积 | 集气瓶中的水: 冷却溅落熔融物, 防止集气瓶炸裂 | 集气瓶中先装满的水:先排尽瓶中空气并便于观察氧气何时集满。 |
A.AB.BC.CD.D
【题目】某化学实验小组要检测黄铜(铜、锌合金)中金属铜的纯度,同学们取6.5g黄铜样品,向其中分三次共加入15g盐酸溶液,充分反应后测得实验结果如下表:
实验次数 | 1 | 2 | 3 |
盐酸质量 | 5g | 5g | 5g |
氢气质量 | 0.04g | m | 0.02g |
请计算:
(1)第二次实验产生氢气的质量m___________g。
(2)黄铜(铜、锌合金)中金属铜的纯度___________。
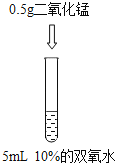
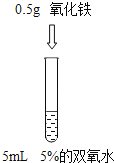
【题目】为了探究”影响双氧水制氧气的速率”的因素,某学习小组设计了下列实验,下列说法正确的是( )
实验① | 实验② | 实验③ |
|
|
|
A. 对比实验②和③,可研究双氧水的质量分数对反应速率的影响
B. 对比实验①和②,可研究双氧水的质量分数对反应速率的影响
C. 对比实验②和③,可研究催化剂的种类对反应速率的影响
D. 对比实验①和②,可研究催化剂的种类对反应速率的影响