题目内容
有两种金属组成的合金6.8克与足量的硫酸溶液反应,产生氢气0.4克,则该合金的组成可能为( )A.Al Mg
B.Na Fe
C.Al Cu
D.Mg Zn
【答案】分析:利用一定质量金属完全反应放出氢气质量= ×金属质量,计算生成0.4g氢气消耗选项所涉及金属铁、锌、镁、铝、钠的质量;然后根据题设的条件:两种金属混合物6.8g,与足量稀硫酸反应后生成了0.4 g氢气,推断出两种金属混合物的可能组成.
×金属质量,计算生成0.4g氢气消耗选项所涉及金属铁、锌、镁、铝、钠的质量;然后根据题设的条件:两种金属混合物6.8g,与足量稀硫酸反应后生成了0.4 g氢气,推断出两种金属混合物的可能组成.
解答:解:根据与硫酸反应时铁、锌、镁、铝、钠分别呈+2、+2、+2、+3、+1价,与足量稀硫酸反应后生成了0.4g氢气,所需要消耗金属的质量分别为:
需要金属铁的质量=0.4g× =11.2g;需要金属锌的质量0.2g×
=11.2g;需要金属锌的质量0.2g× =13g;需要金属镁的质量=0.4g×
=13g;需要金属镁的质量=0.4g× =4.8g;需要金属铝的质量=0.4g×
=4.8g;需要金属铝的质量=0.4g× =3.6g;需要金属钠的质量=0.4g×
=3.6g;需要金属钠的质量=0.4g×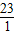 =9.2g,铜不与稀硫酸反应;根据金属混合物与酸反应产生气体质量为两种金属反应产生氢气质量和,由实际实验中两种金属混合物6.8g与足量稀硫酸反应后生成了0.4g氢气,可判断选项混合物中两种金属只可能为金属铜与铝的混合物或镁和锌的混合物;
=9.2g,铜不与稀硫酸反应;根据金属混合物与酸反应产生气体质量为两种金属反应产生氢气质量和,由实际实验中两种金属混合物6.8g与足量稀硫酸反应后生成了0.4g氢气,可判断选项混合物中两种金属只可能为金属铜与铝的混合物或镁和锌的混合物;
故选CD
点评:一定质量金属完全反应放出氢气质量= ×金属质量,利用该公式进行计算时,需要注意到铁在与酸发生置换反应时呈现出+2价.
×金属质量,利用该公式进行计算时,需要注意到铁在与酸发生置换反应时呈现出+2价.
 ×金属质量,计算生成0.4g氢气消耗选项所涉及金属铁、锌、镁、铝、钠的质量;然后根据题设的条件:两种金属混合物6.8g,与足量稀硫酸反应后生成了0.4 g氢气,推断出两种金属混合物的可能组成.
×金属质量,计算生成0.4g氢气消耗选项所涉及金属铁、锌、镁、铝、钠的质量;然后根据题设的条件:两种金属混合物6.8g,与足量稀硫酸反应后生成了0.4 g氢气,推断出两种金属混合物的可能组成.解答:解:根据与硫酸反应时铁、锌、镁、铝、钠分别呈+2、+2、+2、+3、+1价,与足量稀硫酸反应后生成了0.4g氢气,所需要消耗金属的质量分别为:
需要金属铁的质量=0.4g×
 =11.2g;需要金属锌的质量0.2g×
=11.2g;需要金属锌的质量0.2g× =13g;需要金属镁的质量=0.4g×
=13g;需要金属镁的质量=0.4g× =4.8g;需要金属铝的质量=0.4g×
=4.8g;需要金属铝的质量=0.4g× =3.6g;需要金属钠的质量=0.4g×
=3.6g;需要金属钠的质量=0.4g×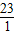 =9.2g,铜不与稀硫酸反应;根据金属混合物与酸反应产生气体质量为两种金属反应产生氢气质量和,由实际实验中两种金属混合物6.8g与足量稀硫酸反应后生成了0.4g氢气,可判断选项混合物中两种金属只可能为金属铜与铝的混合物或镁和锌的混合物;
=9.2g,铜不与稀硫酸反应;根据金属混合物与酸反应产生气体质量为两种金属反应产生氢气质量和,由实际实验中两种金属混合物6.8g与足量稀硫酸反应后生成了0.4g氢气,可判断选项混合物中两种金属只可能为金属铜与铝的混合物或镁和锌的混合物;故选CD
点评:一定质量金属完全反应放出氢气质量=
 ×金属质量,利用该公式进行计算时,需要注意到铁在与酸发生置换反应时呈现出+2价.
×金属质量,利用该公式进行计算时,需要注意到铁在与酸发生置换反应时呈现出+2价. 
练习册系列答案
 天天练口算系列答案
天天练口算系列答案
相关题目
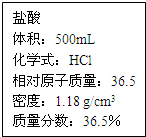 实验室有一瓶浓盐酸,瓶上标签如图所示,请你根据标签上提供的数据解答下列问题.
实验室有一瓶浓盐酸,瓶上标签如图所示,请你根据标签上提供的数据解答下列问题.