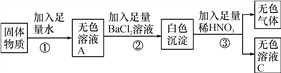
题目内容
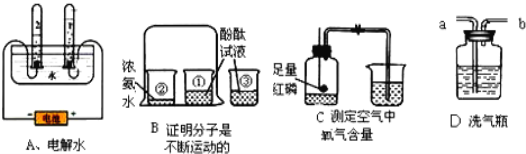
【题目】结合下图所示实验装置回答问题:

⑴写出上图①、②两种仪器的名称:①________________ ② ________________
写出仪器③的主要用途 ____________________
⑵实验室若用高锰酸钾制取氧气,可选用的发生装置是_____和收集装置是____(填标号),反应的文字表达式(或写化学符号)为_____________________________
装置B试管口略向下倾斜的原因是___________用排水法集气后,检验氧气的方法是_______装满氧气的集气瓶瓶口应________(填“向上”或“向下”)放在桌面上。
⑶装置A与C组合,可以制取多种气体:
①若制取氧气,反应的文字表达式为(或写化学符号)_____________________
②若制取二氧化碳,反应的文字表达式(或写化学符号)为______________________
A中长颈漏斗的下端管口如果没有伸到液面以下将造成的后果是__________________
能用装置C收集该气体的原因是___________________、_______________________
⑷若要制取氧气并粗略测定体积,需将上述B、E、F装置进行组装,则导管口的连接顺序为a→_____→_____→b。
【答案】 长颈漏斗 铁架台 量取液体的体积 B C或F 高锰酸钾![]() 锰酸钾+氧气+二氧化锰 防止试管口处的冷凝水倒流炸裂试管 将带火星的木条伸入集气瓶内,木条复燃,则是氧气 向上 【答题空10】过氧化氢
锰酸钾+氧气+二氧化锰 防止试管口处的冷凝水倒流炸裂试管 将带火星的木条伸入集气瓶内,木条复燃,则是氧气 向上 【答题空10】过氧化氢![]() 水+氧气 碳酸钙+盐酸→氯化钙+水+二氧化碳 生成的气体从长颈漏斗中逸出 密度比空气的密度大 不与空气中成分反应 d c
水+氧气 碳酸钙+盐酸→氯化钙+水+二氧化碳 生成的气体从长颈漏斗中逸出 密度比空气的密度大 不与空气中成分反应 d c
【解析】(1)仪器①为长颈漏斗,②为铁架台,③为量筒,主要用于量取液体的体积;
(2)实验室用高锰酸钾制取氧气时需要加热,应该用B装置作为发生装置;因为氧气的密度比空气大,可以用向上排空气法收集,即用C装置收集,氧气不易溶于水,可以用排水法收集,即用F装置收集;加热高锰酸钾分解生成锰酸钾、二氧化锰和氧气,反应的文字表达式是:高锰酸钾![]() 锰酸钾+氧气+二氧化锰;防止试管口处的冷凝水倒流炸裂试管,所以装置B试管口略向下倾斜;由于氧气有助燃性,可将带火星的木条伸入集气瓶内,观察木条是否复燃检验气体是否是氧气;由于氧气的密度大于空气,装满氧气的集气瓶瓶口应向上放在桌面上;
锰酸钾+氧气+二氧化锰;防止试管口处的冷凝水倒流炸裂试管,所以装置B试管口略向下倾斜;由于氧气有助燃性,可将带火星的木条伸入集气瓶内,观察木条是否复燃检验气体是否是氧气;由于氧气的密度大于空气,装满氧气的集气瓶瓶口应向上放在桌面上;
(3)①B装置属于固+液常温型,过氧化氢在二氧化锰的催化作用下制取氧气可用此发生装置,反应的文字表达式是:过氧化氢![]() 水+氧气;
水+氧气;
②实验室制取CO2,是在常温下,用大理石或石灰石和稀盐酸制取的,碳酸钙和盐酸互相交换成分生成氯化钙和水和二氧化碳,因此不需要加热,反应的文字表达式是:碳酸钙+盐酸→氯化钙+水+二氧化碳;
③长颈漏斗的下端管口如果没有伸到液面以下造成的后果是:生成的气体从长颈漏斗中逸出;
④能用装置C收集该气体的原因是密度比空气的密度大,不与空气中成分反应;
(4)若要制取氧气并通过排水量来测定所收集到氧气的体积,整套实验装置接口的正确连接顺序为a→d→c→b;因为氧气不易溶于水,因此可以用F装置收集氧气。

【题目】某研究小组为探究“影响铁制品锈蚀快慢的因素”,取同浓度的稀氨水和稀醋酸,用右图装置完成表中实验,回答下列问题。
![]()
实验序号 | ① | ② | ③ | ④ |
实验温度/℃ | 25 | 25 | 70 | 70 |
试剂 | 稀氨水 | 稀醋酸 | 稀氨水 | 稀醋酸 |
出现铁锈 所需时间 | 1天 未见锈蚀 | 5分钟 | 1天 未见锈蚀 | 1分钟 |
(1)铁锈的主要成分是________(填化学式)。
(2)实验②和④可探究________因素对铁制品锈蚀快慢的影响;欲探究试剂酸碱性对铁制品锈蚀快慢的影响,应选择的实验是______________(填实验序号)。
(3)根据表中实验现象得出的结论是_________________(写出1点即可)。
(4)影响铁制品的锈蚀快慢除上述因素外,还有______________________(写出1点即可),请设计实验方案_________________________________________________。
【题目】苏打水是一种很受欢迎的饮料(如图)。某研究小组进行了如下探究:

探究一:苏打水的酸碱性。
【提出猜想】苏打水可能是一种碱性的饮料。
【设计实验】
编号 | 实验操作 | 实验现象 |
① | 倒入少量苏打水于试管中,滴加无色酚酞试液 | ___________________________ |
② | 将pH试纸直接伸到苏打水中,与标准比色卡对照 | pH____(填“>”“=”或“<”)7 |
【得出结论】苏打水显碱性。
【评价】在上述实验操作步骤________中有不正确的操作,正确的方法是__________________。
【查阅资料】苏打水呈弱碱性。人体内环境是弱碱性。我们每天吃的大多食物都是酸性。因此,需要进行酸碱平衡。
探究二:苏打水的主要成分。
【提出猜想】苏打水主要成分是含有碳酸氢根的钠盐。
【设计实验】
编号 | 实验操作 | 实验现象 |
③ | 倒入少量苏打水于试管中,滴加稀盐酸 | 有气泡产生 |
④ | 将产生的气体通入澄清石灰水中 | __________________ |
【得出结论】
(1)苏打水中含有碳酸氢根离子。
(2)写出编号④发生反应的化学方程式________________________________。
【查阅资料】苏打水是碳酸氢钠的水溶液。请再举出碳酸氢钠的一种用途:________________。