题目内容
【题目】纳米铜粉不仅可以作为催化剂直接应用于化工行业(如乙烯聚合),而且是高导电率、高强度纳米材料不可缺少的基础材料,其性质引起电子界的极大兴趣。某研究性学习小组以废黄铜丝(铜、锌合金)为原料,制备纳米铜粉,其流程如下:
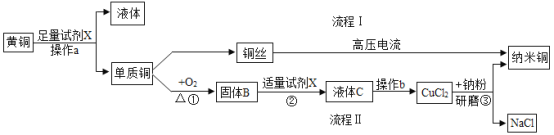
(1)试剂X的化学式为______________________,固体B的化学式为____________________。
(2)操作a所需的玻璃棒作用是___________________;操作b需用玻璃棒不断搅拌,其作用是________________________。
(3)写出反应②的化学方程式________________________;反应③属于_____________反应(填反应类型);
(4)制备纳米铜流程中,流程I是________________(填“物理”或“化学”)变化。
【答案】HCl CuO 引流 防止局部温度过高,造成液滴飞溅 ![]() 置换 物理
置换 物理
【解析】
黄铜为铜、锌合金,加入足量试剂X,可得单质铜和液体,锌能与酸反应生成可溶性锌盐,铜不与酸反应,故X应为酸,铜与氧气在加热的条件下反应生成氧化铜,故B为氧化铜,氧化铜与试剂X形成液体C,液体C经过操作b得到CuCl2,由液体得到固体,故操作b应为蒸发,液体C应为氯化铜溶液,氧化铜能与稀盐酸反应生成氯化铜,故X为盐酸。
(1)试剂X为盐酸。化学式为:HCl;固体B为氧化铜,化学式为:CuO;
(2)操作a实现了固液分离,故操作a为过滤,过滤中玻璃棒的作用是:引流;
操作b为蒸发,蒸发过程中需要用玻璃棒不断搅拌,防止局部温度过高,造成液滴飞溅;
(3)反应②为氧化铜与稀盐酸反应生成氯化铜和水,该反应的化学方程式为:![]() ;
;
反应③为钠粉与氯化铜在研磨的条件下反应生成铜和氯化钠,该反应符合“一种单质与一种化合物反应生成另一种单质和另一种化合物”的反应,属于置换反应;
(4)流程I是铜丝在高压电流的条件下生成纳米铜,纳米铜和铜丝都是由铜原子组成,无新物质生成,属于物理变化。