题目内容
【题目】某化学兴趣小组的同学用如图所示的装置测定空气中氧气的含量,请回答下列问题: 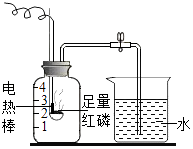
(1)装置中电热棒的作用是;
(2)红磷燃烧一段时间后,自动熄灭了,你认为原因是;红磷燃烧的化学方程式;
(3)足量红磷充分燃烧后冷却至室温,打开止水夹,观察到水沿导管进入集气瓶,水进入集气瓶其原因是;进入集气瓶的水约为集气瓶容积的五分之一,由此你得出的结论是
【答案】
(1)引燃红磷
(2)瓶内氧气已耗尽;4P+5O2 ![]() 2P2O5
2P2O5
(3)红磷燃烧消耗了瓶内的氧气.生成物数固体,瓶内压强下雨大气压;氧气约占空气体积的五分之一
【解析】解:测定空气中氧气的含量实验原理:利用红磷燃烧消耗空气中的氧气,使左边集气瓶内气体体积变小,压强变小,从而在外部大气压的作用下使烧杯内的水进入集气瓶,通过测量进入集气瓶中水的量来确定空气中氧气的体积分数.(1)要想让红磷燃烧消耗空气中的氧气就要点燃红磷,故装置中电热棒的作用是点燃红磷;故答案为:引燃红磷;(2)红磷燃烧一段时间后,自动熄灭了,原因是瓶内氧气已耗尽,红磷燃烧生成五氧化二磷,反应的化学方程式为:4P+5O2 ![]() 2P2O5 ;故答为:瓶内氧气已耗尽,4P+5O2
2P2O5 ;故答为:瓶内氧气已耗尽,4P+5O2 ![]() 2P2O5 ;(3)由上面的分析可知水进入集气瓶的原因是:红磷燃烧消耗了集气瓶中的氧气,瓶内气体压强减小;得出的结论是:氧气约占空气体积的五分之一;故答案为:红磷燃烧消耗了集气瓶中的氧气,瓶内气体压强减小,氧气约占空气体积的五分之一. (1)从要想让红磷燃烧消耗空气中的氧气就要点燃红磷去分析解答(2)根据氧气能支持燃烧和红燃烧的反应分析回答;(3)从测定空气中氧气的含量实验原理去分析解答.
2P2O5 ;(3)由上面的分析可知水进入集气瓶的原因是:红磷燃烧消耗了集气瓶中的氧气,瓶内气体压强减小;得出的结论是:氧气约占空气体积的五分之一;故答案为:红磷燃烧消耗了集气瓶中的氧气,瓶内气体压强减小,氧气约占空气体积的五分之一. (1)从要想让红磷燃烧消耗空气中的氧气就要点燃红磷去分析解答(2)根据氧气能支持燃烧和红燃烧的反应分析回答;(3)从测定空气中氧气的含量实验原理去分析解答.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目