题目内容
要除去下列物质中的少量杂质(括号内为杂质),写出所用试剂和有关的化学方程式:
| 物质 | 所用试剂 | 化学方程式 | ||||||||
| FeSO4(CuSO4) | 铁 铁 |
Fe+CuSO4═FeSO4+Cu Fe+CuSO4═FeSO4+Cu | ||||||||
| NaNO3(NaCl) | 硝酸银溶液 硝酸银溶液 |
NaCl+AgNO3═NaNO3+AgCl↓ NaCl+AgNO3═NaNO3+AgCl↓ | ||||||||
| NaOH(Na2CO3) | 氢氧化钙溶液 氢氧化钙溶液 |
Ca(OH)2+Na2CO3═CaCO3↓+2NaOH Ca(OH)2+Na2CO3═CaCO3↓+2NaOH | ||||||||
| CaO(CaCO3) | 无 无 |
CaCO3
CaCO3
|
分析:根据原物质和杂质的性质选择适当的除杂剂和分离方法,所谓除杂(提纯),是指除去杂质,同时被提纯物质不得改变.除杂质题至少要满足两个条件:①加入的试剂只能与杂质反应,不能与原物质反应;②反应后不能引入新的杂质.
解答:解:要除去FeSO4溶液中的CuSO4,实质就是除去铜离子,可利用铁与硫酸铜溶液反应生成硫酸亚铁溶液和铜,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Fe+CuSO4═FeSO4+Cu.
要除去NaNO3溶液中的NaCl,实质就是除去氯离子,可利用氯化钠溶液与硝酸银反应生成氯化银沉淀和硝酸钠溶液,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:NaCl+AgNO3═NaNO3+AgCl↓.
要除去NaOH溶液中的Na2CO3,实质就是除去碳酸根离子,可利用碳酸钠溶液与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠溶液,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
CaCO3在高温下分解生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:CaCO3
CaO+CO2↑.
故答案为:
要除去NaNO3溶液中的NaCl,实质就是除去氯离子,可利用氯化钠溶液与硝酸银反应生成氯化银沉淀和硝酸钠溶液,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:NaCl+AgNO3═NaNO3+AgCl↓.
要除去NaOH溶液中的Na2CO3,实质就是除去碳酸根离子,可利用碳酸钠溶液与氢氧化钙反应生成碳酸钙沉淀和氢氧化钠溶液,然后过滤即可,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:Ca(OH)2+Na2CO3═CaCO3↓+2NaOH.
CaCO3在高温下分解生成氧化钙和二氧化碳,能除去杂质且没有引入新的杂质,符合除杂原则,反应的化学方程式为:CaCO3
| ||
故答案为:
| 物质 | 所用试剂 | 化学方程式 | ||||
| FeSO4(CuSO4) | 铁 | Fe+CuSO4═FeSO4+Cu | ||||
| NaNO3(NaCl) | 硝酸银溶液 | NaCl+AgNO3═NaNO3+AgCl↓ | ||||
| NaOH(Na2CO3) | 氢氧化钙溶液 | Ca(OH)2+Na2CO3=CaCO3↓+2NaOH | ||||
| CaO(CaCO3) | 无 | CaCO3
|
点评:物质的分离与除杂是中考的重点,也是难点,解决除杂问题时,抓住除杂质的必需条件(加入的试剂只与杂质反应,反应后不能引入新的杂质)是正确解题的关键.

练习册系列答案
 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案
相关题目
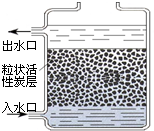 2003年6月5日世界环境日的主题为:“水-20亿人生命之所系”.请你参与下列有关问题的讨论:
2003年6月5日世界环境日的主题为:“水-20亿人生命之所系”.请你参与下列有关问题的讨论: