题目内容
【题目】下列仪器不宜用作化学反应容器的有
A.试管 B.烧杯 C.燃烧匙 D.量筒
【答案】D
【解析】
试题分析:量筒只能用来量取液体的体积,不能加热也不能作为反应容器。故选D。

 培优好卷单元加期末卷系列答案
培优好卷单元加期末卷系列答案【题目】下表列出了固体物质A在不同温度时的溶解度:
温度/℃ | 0 | 10 | 20 | 30 | 40 | 50 | 60 | 70 | 80 | 90 |
溶解度/g | 36 | 35 | 34 | 33 | 32 | 31 | 30 | 29 | 28 | 27 |
(1)70℃时,向盛有100g水的烧杯中加入30g固体A,充分溶解形成的是______________(填“饱和”或“不饱和”)溶液,再将烧杯内物质温度降至20℃,此时溶液中溶质与溶剂的质量比为_____________(填最简整数比);
(2)通过对上表数据的分析,物质A的溶解度曲线应是右图中的___________(填“甲”或“乙”);

(3)80℃时,配制一定量A物质的溶液,将其降温到60℃,是否有固体析出?____________(填“有”、 “没有”或“不确定”)。
【题目】(1)为证明中和反应是放热反应,某小组进行了如图所示的实验操作:
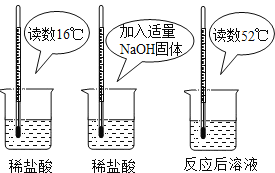
根据如图实验,甲同学认为:NaOH与稀盐酸发生的中和反应是放热反应.乙同学认为:甲同学得出这个结论的依据不科学,理由是_____________________________。丙同学认为:通过多个实验才能得出一个普遍的结论。请你再举出一个酸碱中和反应的实例,写出反应的化学方程式_____________________________。
(2)为探究影响中和反应放出热量多少的因素,他们又进行了如下实验:在编号为A、B、C、D、E的五只烧杯中各装入36.5g溶质质量分数为5%、10%、15%、20%、25%的盐酸,再向上述五只烧杯中分别加入40g20%的氢氧化钠溶液,最后测量其温度,数据记录如下:
烧杯编号 | A | B | C | D | E |
盐酸的溶质质量分数 | 5% | 10% | 15% | 20% | 25% |
反应后溶液温度(℃) | 24℃ | 34℃ | 46℃ | 54℃ | 54℃ |
【实验结论】影响中和反应放出热量多少的因素是____________________________。
【交流反思】反应后,烧杯内溶液pH最小的是______(填烧杯编号)。
若要使40g20%的氢氧化钠溶液恰好完全中和,则需要10%的盐酸溶液多少克?(根据化学方程式列式计算)__________