题目内容
【题目】在宏观、微观、符号之间建立联系,是化学学科特有的思维方式。
(1)在C60、金刚石、硫酸铜三种物质中,由分子构成的物质是 。
(2)用符号完成下面问题:
①由一种原子形成的两种不同离子 ;
②含有两种相同原子的两种不同离子 。
(3)从微观角度解释下列问题:
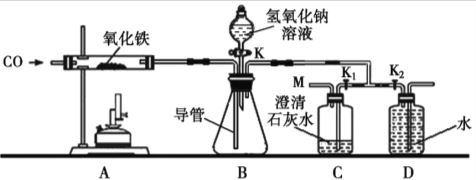
①一氧化碳和二氧化碳化学性质不同的原因是 ;
②金刚石和石墨物理性质差异很大的原因是 。
(4)右图表示核电荷数为11~17的元素最高和最低化合价。

① 从图中可知,硫元素的最高正价氧化物的化学式为 。
② 若某元素既可显正价,又可显负价,则最高正价与最低负价绝对值的代数和为 。
(5)具有相同原子数和电子数的分子或离子叫等电子体,等电子体具有相似的结构和性质。下列各组微粒中属于等电子体的是 (填字母序号)。
A.NO和O2 B.CO和N2 C.SO2和CO2 D.H2O和NH3
(6)在点燃条件下,A和B反应生成C和D。反应前后分子变化的微观示意图如下所示。

①写出该反应的化学方程式 。
②该反应中,A、C两种物质的质量变化之比为 。
【答案】(1)C60 (2) ①Fe2+ 与 Fe3+ ②MnO4- 与MnO42-
(3)①分子结构不同 ②碳原子排列方式不同。 (4)① SO3
②+8 (5) B(6)①4NH3+3O2 ![]() 2N2+6H2O ② 17:14
2N2+6H2O ② 17:14
【解析】
试题分析:(1)C60由分子构成,金刚石由原子构成,硫酸铜由离子构成,(2)Fe2+与Fe3+是由同种原子形成的两种不同离子,KMnO4-与KmnO42-是含有两种相同原子的两种不同离子。(3)①结构决定性质,分子结构不同,物质的性质不同。②由于金刚石和石墨的原子排列方式不同,因此它们的性质差异很大。(4)①S元素的最高正价是+6,它的氧化物的化学式是SO3.②因为原子的最外层是8个电子时是一种稳定结构,所以最高正价与最高负价的绝对值的代数和为+8.(5)等电子体既要含有相同的原子数又要含有相同的电子数,CO和 N2符合条件。(6)①根据微观示意图可知,A表示一个NH3,B表示一个O2,C表示一个N2分子,D表示一个H2O分子,所以化学方程式是4NH3+3O2![]() 2N2+6H2O ②A、C两种物质的质量比是:4×17:2×28=17:14
2N2+6H2O ②A、C两种物质的质量比是:4×17:2×28=17:14

 名校课堂系列答案
名校课堂系列答案【题目】已知氯酸钾(KClO3)固体在二氧化锰作催化剂,在加热的条件下也可制得氧气,同时生成氯化钾(KCl)固体。写出该反应的化学方程式: ,该反应的基本类型是 。
小芳发现,氯酸钾与氧化铜混合加热,也能较快产生氧气,于是进行如下探究:
【提出猜想】除MnO2、CuO外,Fe2O3也可以作KClO3分解的催化剂。
【进行实验】按如表进行实验,并测定分解温度(分解温度越低,催化效果越好).
实验编号 | 实验药品 | 分解温度(℃) |
① | K KClO3 | 5 580 |
② | K KClO3、MnO2(质量比1:1) | 3 350 |
③ | K KClO3、CuO(质量比1:1) | |
④ | K KClO3、Fe2O3(质量比1:1) | 3 390 |
【分析数据、得出结论】
(1)由实验 与实验④对比,证明猜想合理;
(2)实验所用的三种金属氧化物比较,氧化铜催化效果仅次于二氧化锰,请你推出其分解温度(用t表示)的取值范围: ;
【交流反思】
(3)若要证明Fe2O3是该反应的催化剂,还要验证它在化学反应前后的 和
不变;
(4)影响氯酸钾分解快慢除催化剂种类外,你认为还可能有的影响因素是
(写出一种即可)。