题目内容
【题目】将12.5g石灰石(杂质不与酸反应也不溶于水),加入到装有100g稀盐酸的烧杯中。恰好完全反应后,烧杯中物质的总质量为108.1g。请计算。
(1)生成二氧化碳的质量为_____g。
(2)求稀盐酸中溶质的质量分数(写出计算过程)_____。
【答案】4.4 7.3%
【解析】
根据质量守恒定律可知,过程中质量的减少是因为生成了二氧化碳,所以可以求算二氧化碳的质量,根据二氧化碳的质量和对应的化学方程式求算稀盐酸中溶质的质量分数。
解:(1)根据质量守恒定律可知反应前后物质总质量不变,所以二氧化碳的质量为:12.5g+100g﹣108.1g=4.4g;
(2)设稀盐酸中溶质的质量分数为x,
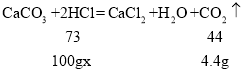
![]()
x=7.3%;
答:(1)生成二氧化碳的质量为4.4g。
(2)稀盐酸中溶质的质量分数为7.3%。

 巧学巧练系列答案
巧学巧练系列答案【题目】(10分)氧气是生产生活中重要的物质。
(1)氧气有很多用途。下列属于氧气用途的是 和 (填序号)。
A.医疗急救 B.食品防腐 C.航天火箭 D.霓虹灯
(2)氧气能跟很多物质反应。根据下图所示实验,并阅读资料,回答下列问题。

Ⅰ.小明对图1铁丝在氧气中燃烧为什么会火星四射进行探究。下表是他将纯镁条和不同含碳量的铁丝(镁条和铁丝直径均为0.4mm)放入氧气中燃烧时的实验现象的记录.请你分析回答:
物质 | 镁条 | 含碳0.05%的铁丝 | 含碳0.2%的铁丝 | 含碳0.6%的铁丝 |
燃烧时 的现象 | 剧烈燃烧,发出 耀眼白光,无火星 | 剧烈燃烧 极少火星 | 剧烈燃烧 少量火星 | 未填 |
①表中“未填”部分的内容应为__ ___;
②铁丝在氧气燃烧的文字表达式是___ 。
集气瓶底部放少量水或细沙的作用是______________________
③通过以上探究,你认为铁丝燃烧产生火星四射现象的原因可能是__ ____。
Ⅱ.图2中的反应现象为 ,反应的文字表达式为 ,集气瓶中加入的液体可能是 ,其主要目的是___ 。
【题目】玲玲在学习复分解反应时,对复分解反应的条件产生了兴趣,于是她和小组内的同学仅用以下药品展开了探究活动。
实验药品:稀H2SO4、稀HCl、NaOH溶液、Na2CO3溶液、Ba(NO3)2溶液、NaCl溶液、酚酞溶液
(提出问题)复分解反应发生的条件是什么?
(查阅资料)硝酸钡溶液显中性,且Ba2+有毒。
(实验探究)玲玲用上述物质做了下列几组实验。
组合序号 | ① | ② | ③ | ④ | ⑤ | ⑥ |
组合物质 | H2SO4 NaOH | H2SO4 NaCl | H2SO4 Na2CO3 | H2SO4 Ba(NO3)2 | NaOH Ba(NO3)2 | Na2CO3 Ba(NO3)2 |
(记录和解释)(1)组合①、②、⑤均无明显现象,其中组合_____与另外两组的实质不同。为证明该不同之处,玲玲在实验过程中使用了酚酞溶液。
(2)请写出组合④的化学方程式_____________。
(实验结论)他们请教老师并讨论后知道,只有当两种化合物互相交换成分,生成物中有沉淀或水或气体生成时,复分解反应才可以发生。
(应用)写出利用熟石灰鉴别化肥氯化铵和氯化钾有关反应的化学方程式_______________________。
(拓展延伸)实验结束后,他们将所有废液收集在废液缸中静置,观察到白色沉淀和无色的上层清液。
为了确定沉淀和清液的成分,继续展开探究。
(实验1)探究沉淀的成分。
(提出猜想)Ⅰ.沉淀只有BaSO4 Ⅱ.沉淀只有BaCO3 Ⅲ.沉淀中含有BaSO4和BaCO3。
梅梅取少量沉淀于试管中,滴加过量的______,观察到沉淀部分溶解,证明了猜想Ⅲ是正确的。
(实验2)探究清液的成分。
①取少量清液于试管中,向其中滴加几滴硝酸钡溶液,无明显现象。
②另取少量清液于另一只试管中,滴加几滴______________,有白色沉淀产生。
(解释与结论)探究活动结束后,小组内成员通过讨论分析,一致认为清液中含有的离子除Na+、Cl-外,还有____________________(指示剂除外)。
(处理废液)为了防止污染环境,玲玲向废液缸中加入适量的_________,对废液进行处理后,将固体回收进一步处理,溶液排放。
(交流与反思)根据你对物质溶解性的了解,结合复分解反应发生的条件,请写出一种在水溶液中一般不能发生复分解反应的可溶性盐_____________(写化学式)。