题目内容
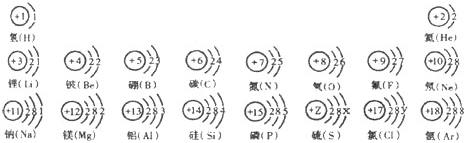
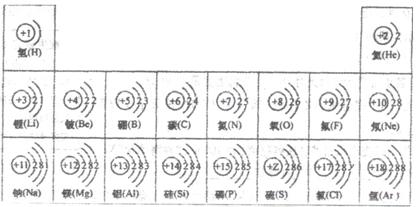
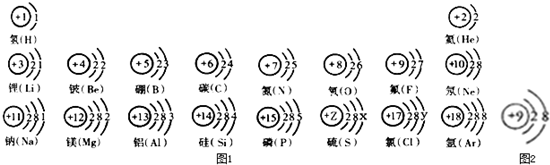
依据核电荷数为1-18的元素的原子结构示意图,回答下列问题:
(1)在图中硫元素的核电荷数z=______;氯元素的最外层电子数Y=______ (填数值),则与氯元素化学性质相似的元素是______.
(2)核电荷数为12的元素的原子失去两个电子后,符号为______.该粒子的核外电子排布与______元素的原子核外电子排布相同.
(3)上图的排列具有一定的规律,如:同一行中,从左到右元素的核电荷数依次增加.你还能找到哪些规律?(至少写两个)
(4)现有质量相等的铜、锌、铁三块金属,原子个数由多到少的顺序是______.
(5)已知原子核内有6个质子和6个中子的一个碳原子质量为a克,若另一种原子的质量为b克,则另一种原子的相对原子质量为(用a、b表示 )______.
【答案】分析:(1)根据元素周期律:在元素周期表中,同一周期元素从左到右原子序数的逐渐递增,进行解答;
根据在原子中,原子序数=质子数=核外电子数,进行解答;
根据元素周期律:同一纵行,原子最外层电子数相同,最外层电子数相同的元素化学性质相似,进行解答;
(2)根据离子符号的表示法:在元素符号的右上角标明离子所带电荷数及电性,及离子示意图找出相同的结构,进行解答;
(3)根据图中所给的信息及其规律进行解分析解答本题.
(4)依据相对原子质量与原子的真实质量成正比分析解答;
(5)依据相对原子质量的计算方法分析解答;
解答:解:(1)根据元素周期律:在元素周期表中,同一周期元素从左到右原子序数的逐渐递增,硫元素的核电荷数介于15与17 之间;所以硫元素的核电荷数z=16;
根据在原子中,原子序数=质子数=核外电子数,可得 17=2+8+y,则y=7;
根据元素周期律:同一纵行,原子最外层电子数相同,最外层电子数相同的元素化学性质相似,所以与氯元素化学性质相似的元素是氟;
(2)根据离子符号的表示法:在元素符号的右上角标明离子所带电荷数及电性,所以核电荷数为12的元素的原子失去两个电子后,形成的粒子的符号为:Mg2+;与其离子示意图相同的结构的元素为:Ne;
(3)根据图中所给的信息及其元素周期律可得:同一行中,从左到右元素的最外层电子数依次增加、同一列中,从上到下元素的最外层电子数相同;
(4)依据相对原子质量与原子的真实质量成正比,且三者的相对原子质量的大小关系是Fe<Cu<Zn,所以质量相等的铜、锌、铁三块金属,原子个数由多到少的顺序是Fe>Cu>Zn;
(5)由于相对原子质量= ,所以
,所以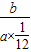 =12
=12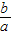
故答案为:
(1)16;7;F;(2)Mg2+;Ne;(3)同一横行,电子层数相同,最外层电子数依次递增.同一纵行,最外层电子数相同,电子层数依次递增.
(4)Fe>Cu>Zn
(5)12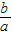
点评:了解原子的定义和构成:原子由原子核和核外电子构成,其中原子核由质子和中子构成的;了解元素周期表的特点及其应用是解题的关键.
根据在原子中,原子序数=质子数=核外电子数,进行解答;
根据元素周期律:同一纵行,原子最外层电子数相同,最外层电子数相同的元素化学性质相似,进行解答;
(2)根据离子符号的表示法:在元素符号的右上角标明离子所带电荷数及电性,及离子示意图找出相同的结构,进行解答;
(3)根据图中所给的信息及其规律进行解分析解答本题.
(4)依据相对原子质量与原子的真实质量成正比分析解答;
(5)依据相对原子质量的计算方法分析解答;
解答:解:(1)根据元素周期律:在元素周期表中,同一周期元素从左到右原子序数的逐渐递增,硫元素的核电荷数介于15与17 之间;所以硫元素的核电荷数z=16;
根据在原子中,原子序数=质子数=核外电子数,可得 17=2+8+y,则y=7;
根据元素周期律:同一纵行,原子最外层电子数相同,最外层电子数相同的元素化学性质相似,所以与氯元素化学性质相似的元素是氟;
(2)根据离子符号的表示法:在元素符号的右上角标明离子所带电荷数及电性,所以核电荷数为12的元素的原子失去两个电子后,形成的粒子的符号为:Mg2+;与其离子示意图相同的结构的元素为:Ne;
(3)根据图中所给的信息及其元素周期律可得:同一行中,从左到右元素的最外层电子数依次增加、同一列中,从上到下元素的最外层电子数相同;
(4)依据相对原子质量与原子的真实质量成正比,且三者的相对原子质量的大小关系是Fe<Cu<Zn,所以质量相等的铜、锌、铁三块金属,原子个数由多到少的顺序是Fe>Cu>Zn;
(5)由于相对原子质量=
 ,所以
,所以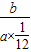 =12
=12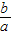
故答案为:
(1)16;7;F;(2)Mg2+;Ne;(3)同一横行,电子层数相同,最外层电子数依次递增.同一纵行,最外层电子数相同,电子层数依次递增.
(4)Fe>Cu>Zn
(5)12
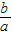
点评:了解原子的定义和构成:原子由原子核和核外电子构成,其中原子核由质子和中子构成的;了解元素周期表的特点及其应用是解题的关键.

练习册系列答案
 新课标同步训练系列答案
新课标同步训练系列答案
相关题目